ヘリコバクター・ピロリとは
ヘリコバクター・ピロリ(Helicobacter pylori:通称ピロリ菌)は、胃の下部(幽門部や前庭部)の粘膜に定着するグラム陰性の細菌です。菌体はらせん状で、大きさは約 0.5 × 2.5–4.0 μmです。数本のべん毛をもち、胃粘液の中を泳ぐことができます[1][図1]。
ピロリ菌は尿素分解酵素(ウレアーゼ)によって周囲の尿素をアンモニアと二酸化炭素に分解することができます。ここで産生されたアンモニアが胃酸を局所的に中和するため、ピロリ菌は強酸性の胃の中でも生存することができます[1]。
「胃は無菌に近い臓器である」、「胃潰瘍や胃炎はストレスや食生活などを主因とした非感染性疾患である」という従来の通説は、ピロリ菌の発見によって根底から覆されました。
発見の歴史と医学へのインパクト
ピロリ菌を人間の胃から単離し、培養して、その臨床的意義を示したのは、オーストラリアの病理医 Robin Warren と内科研究医 Barry J. Marshall です。1983–1985年にかけてヒトの胃から菌を発見し、Campylobacter pylori(キャンピロバクター・ピロリ)と命名しました。これが後にヘリコバクター・ピロリと呼ばれるようになりました[1]。
胃は無菌であるという通説に対し、Marshallは自らピロリ菌の培養液を飲み、自身に一時的な急性胃炎を起こすことで、ピロリ菌の存在、そしてピロリ菌感染が胃炎などの胃粘膜病変の原因になることを実証しました[2]。
その後、ピロリ菌の病原性を示す研究成果が蓄積し、彼らは2005年にノーベル医学・生理学賞「ピロリ菌の発見および胃炎・胃潰瘍への関与の解明」を受賞しました[1]。
この発見は、「胃にも細菌感染症があり、除菌がその疾患の発症の予防に繋がりうる」という新たなパラダイムを医療に生み出しました。
疫学および臨床像
- ピロリ菌は世界中に広く分布し、世界人口の約半数に感染していると推定されます。多くの場合、ピロリ菌感染は免疫が不完全な幼少期に始まり、そのまま胃粘膜にピロリ菌が定着した状態が長期に続きます[1]。
- 疫学や臨床の研究成果から、ピロリ菌の長期感染は慢性胃炎や胃・十二指腸潰瘍の原因になることが示されています。
- 感染がさらに長期になると、萎縮性胃炎、腸上皮化生(胃上皮が腸上皮のように変化する)を経て、胃がんに進展することがあります。また、ピロリ菌感染は胃MALTリンパ腫の原因になることも知られています[3]。
- 近年のメタ解析や長期コホート研究から、感染者に対して除菌を行うと、胃がんの発生や胃がんによる死亡のリスクが低下することが示されています[4]。現在では、胃酸分泌抑制薬と抗生物質を1週間服用する除菌プロトコルが推奨され、約8〜9割の成功率で除菌が達成されています[5]。
一方で、除菌を完了しても、これらの疾患のリスクがどの程度小さくなるかは、個々の場合によって異なります。例えば、胃粘膜の萎縮や腸上皮化生の程度が大きい場合には、除菌後も胃がん発症のリスクが残ると考えられています[6]。
ピロリ菌の感染はなぜ「胃がんの原因」と考えられるのか?
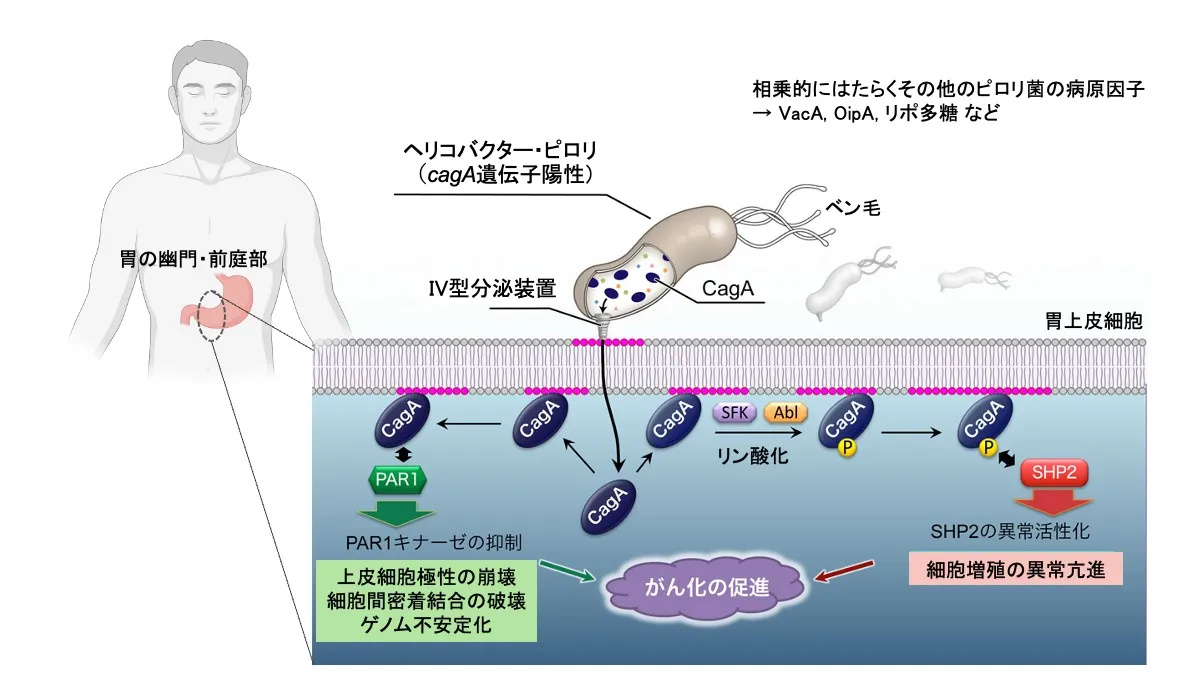
今日では、「ピロリ菌感染は胃がん発症の主な要因」という考えが通説になっています。その背景には、ピロリ菌の病原性タンパク質CagA(Cytotoxin-associated gene A)の関与があります。cagA遺伝子を持つピロリ菌はミクロの注射針(IV型分泌装置)を用いてヒトの胃上皮細胞にCagAタンパク質を打ち込むのです[図2]。
- CagAはピロリ菌のゲノムのcag病原性領域(cag pathogenicity island, cag PAI)と呼ばれる領域内のcagA遺伝子にコードされており、ピロリ菌内で産生されます。ピロリ菌の感染は胃粘膜病変の発症を促進しますが、中でも、胃がんの発症はcagA遺伝子をもつピロリ菌の感染と強く相関することが知られています[1,7]。
- IV型分泌装置でヒトの胃上皮細胞内に輸送されたCagAは、ヒトの細胞がもつ酵素(SRCキナーゼ)によってリン酸化修飾されます。CagAはリン酸化されることでヒトの発がん促進酵素として知られるSHP2と結合できるようになり、SHP2の酵素活性を制御不能に活性化します。その結果、CagAは胃上皮細胞に増殖異常を引き起こし、正常な胃上皮細胞ががん細胞へと変化することを促進します[7,8]。
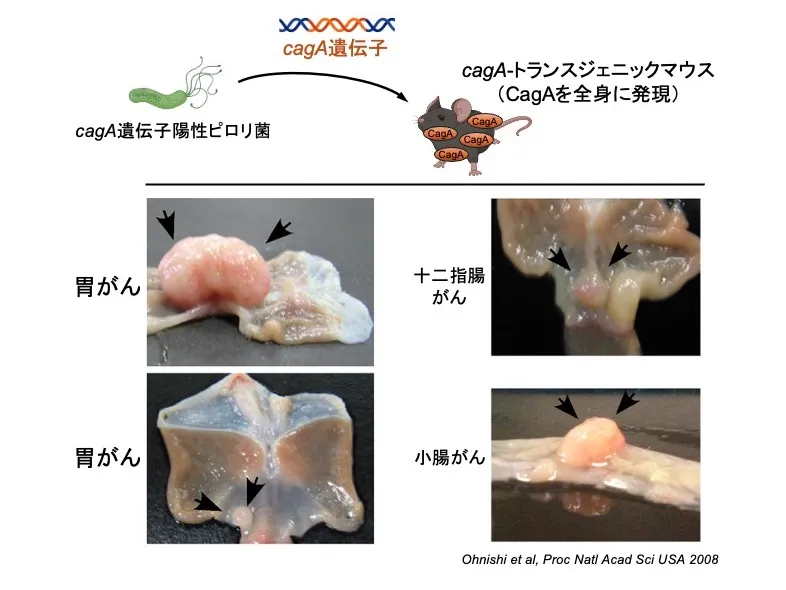
- CagAをマウスの全身の細胞で発現するトランスジェニックマウスでは、胃粘膜の細胞増殖が異常に亢進して胃がんが自然に発症し、また、小腸や血液細胞でも同様に発がんが起こることが報告されています。一方で、正常のマウスではがんが自然発症することはありません。この結果から、CagAは哺乳動物に発がんを起こす能力をもつ、細菌由来の発がん促進タンパク質(bacterial oncoprotein)であることが実証されました[7,9]。
以上より、ピロリ菌、特にcagA遺伝子をもつピロリ菌の感染は、今や慢性炎症のみならず、胃がんの原因として理解されるようになりました[1,7]。また、ピロリ菌はCagAに加えて、細胞傷害性の病原因子[空胞化毒素(VacA)、DupA、ムチナーゼ、プロテアーゼ、リパーゼなど]や炎症を引き起こす病原因子[OipA、リポ多糖など]をもつことが知られています。CagAとこれらの病原因子の相乗的な作用がピロリ菌の病原活性の本態であると考えられています[1,7]。
ピロリ菌研究を国際的に先導する日本人研究者による革新的な成果
日本・中国・韓国を含む東アジアは胃がんの最多発地域であり、その頻度は欧米の約5〜10倍にのぼります[10]。これを背景に、世界のピロリ菌研究は多くの日本人研究者によって牽引されてきた歴史をもちます。ここでは、そのいくつかの成果をご紹介します。
「胃がんはピロリ菌感染者から生じる」ことを明らかに:上村直実博士
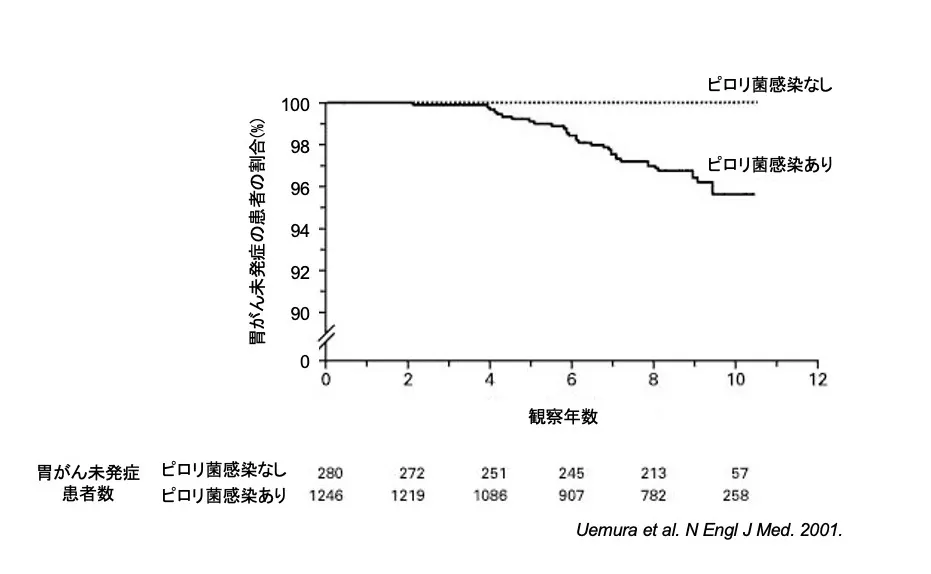
- ピロリ菌感染と胃がん発症の関連を前向きに検証する疫学研究を行いました。胃に疾患をもつ成人患者(約1500名)を対象に、約8年間にわたり数年ごとに内視鏡検査を行いました。その結果、ピロリ菌感染者から胃がん発症者が生じ、ピロリ菌の感染がない患者からは1例も胃がんが発症しませんでした。この研究から、「ピロリ菌感染が胃がん発症のリスクである」ことが明確に示されました[11][図3]。
この成果は、「ピロリ菌感染者は(たとえ無症状であっても)除菌することで、胃がんの予防につながりうる」ことを示唆する重要なエビデンスになりました[11]。ピロリ菌感染のスクリーニングやピロリ菌除菌の戦略(衛生改善による幼少期感染の一次予防や除菌後再感染の二次予防など)といった、今日行われている胃がん・胃疾患の予防策はいずれもこの成果をもとに設計されました[3]。
「CagAの発がん活性」を分子レベルで明らかに:畠山昌則博士
- 胃上皮細胞内でリン酸化されたCagAが、血液がんの原因分子として知られるSHP2と結合し、この結合によってSHP2の酵素活性が、血液がんの場合と同様に、制御不能状態に活性化することを発見しました[7,8]。
- CagAの3次元立体構造を明らかにし、胃がん発症頻度が高い東アジアのピロリ菌がもつCagAは、発症頻度の低い欧米のピロリ菌のCagAと比較して、約100倍強くSHP2を活性化する構造をもつことを明らかにしました[7,12,13]。
- CagAが上皮細胞極性を制御するキナーゼ(PAR1b)と結合し、その酵素活性を阻害することを発見しました。このCagAによるPAR1bの不活性化は、胃上皮細胞の細胞極性や細胞間密着結合(タイトジャンクション)を崩壊させ、同時に遺伝子変異を蓄積させることを明らかにしました[7,14,15]。
- CagAを全身に発現するトランスジェニックマウスを独自に作出し、CagAが哺乳動物の胃や小腸にがんを起こす能力をもつことを世界で初めて実証しました[7,9,16][図4]。
ヒト胃上皮の培養細胞やマウスの胃粘膜にCagAを発現する独自の実験系で、CagAが胃上皮細胞のシグナル伝達系を攪乱することを証明しました[7]。一連の成果から、ピロリ菌感染と胃発がんの因果関係が分子レベルで理解できるようになりました。
ピロリ菌の多様性・進化の解明と胃がん撲滅に向けた国際先導:山岡吉生博士
- 国際共同研究チームを先導して、世界各地から収集した約7000のヘリコバクター属のゲノムデータを大規模比較解析し、ピロリ菌の地球規模での地理的拡散と遺伝的多様性獲得の歴史を紐解きました。ピロリ菌は人類とともに数十万年前のアフリカに起源をもち、感染者の食生活などの影響を受けながら遺伝的多様性を獲得し、世界中に拡散してきた可能性を提示しました。人類の移動・食性・環境適応とピロリ菌が長期間にわたり共進化してきたことが示唆されています[17-19]。
この成果から、ピロリ菌の遺伝型に加えて、感染者の地域特性・民族特性・環境特性などの多因子を対象にした多次元解析が実現でき、より解像度の高いリスク層別化が可能になります。実際に、これを土台として個々の感染に対してより有効な公衆衛生戦略・除菌プロトコル・ワクチン戦略・分子標的治療に繋げる取り組みとして、胃がん死亡率が世界3位のブータンで国をあげた胃がん撲滅プロジェクトを先導しています[20]。
まとめ
ピロリ菌は、胃という過酷な酸性環境でも生存するユニークな細菌であり、その発見は胃疾患・胃がんの発症メカニズムの概念を大きく変えました。特に、CagAという発がん促進分子をもつピロリ菌株の存在は、胃がんを「感染由来がん」と捉える科学的根拠となり、発がん分子メカニズム・動物モデル・疫学・臨床治験・予防プロトコルの研究を加速させ、今日の胃がん対策・公衆衛生戦略の土台となりました。
ピロリ菌そして胃がんの根絶を目指す、日本が牽引するピロリ菌研究の進展にますます目が離せません。
記事執筆:金光(髙橋)昌史(順天堂大学大学院医学研究科 助教/専門 発がん分子機序解析・がんの3次元組織イメージング)
なぜ日本人は胃がんになりやすい?ピロリ菌の発がん実行犯「CagA」の発がん分子メカニズムを解明
参考文献
- Wikipedia ヘリコバクター・ピロリ
- 実験のために約10億個のピロリ菌を飲んだ男
- Y. Uno. Cancer Med. 2019 Jul;8(8):3992-4000.
- A. C. Ford et al. Cochrane Databases Syst Rev. 2020 Jul 6;7(7):CD005583.
- ピロリ菌関連情報 日本ヘリコバクター学会
- K. Mizukami et al. Cancers. 2025 17(3), 552.
- A. Takahashi-Kanemitsu et al. Cell & Mol Immunol. 2020 15, 50-63.
- H. Higashi et al. Science. 2002 295(5555), 683-686.
- N. Ohnishi et al. Proc Natl Acad Sci USA. 2008 105(3), 1003-1008.
- http://globocan.iarc.fr/factsheets/cancers/stomach.asp
- N. Uemura et al. N Eng J Med. 2001 345, 784-789.
- T. Hayashi et al. Cell Host Microbe. 2012 12(1), 20-33.
- T. Hayashi et al. Cell Rep. 2017 20(12), 2876-2890.
- I. Saadat et al. Nature. 2007 447, 330-333.
- S. Imai et al. Cell Host Microbe. 2021 29(6), 941-958.
- A. Takahashi-Kanemitsu et al. Sci Signal. 2023 16(794), eabp9020.
- D. Falush et al. Science. 2003 299(5612), 1582-1585.
- B. Linz et al. Nature. 2007 445(7130), 915-918.
- E. Tourrette et al. Nature. 2024 635, 178-185.
- SATREPSプロジェクト(ピロリ菌感染症関連死撲滅に向けた中核拠点形成事業)
(上記すべて参照:2026-3-19)