リケラボは研究者、研究開発・技術職など理系の知識を生かしてはたらきたい人を応援する情報サイトです。

なぜ日本人は胃がんになりやすい?ピロリ菌の発がん実行犯「CagA」の発がん分子メカニズムを解明
想定外のデータを捨てずに深堀り、新発見
胃がんの大きなリスク要因のひとつにヘリコバクター・ピロリ(ピロリ菌)が挙げられることは、今や広く知られています。しかし、同じようにピロリ菌に感染していても、欧米よりも日本を含む東アジアの方が胃がんの発症率が格段に高いという事実は、長年にわたって世界的な医学ミステリーとされてきました。この「胃がんリスクの東西格差」はなぜ存在するのでしょうか。また、そもそもピロリ菌は、どのように細胞をがん化へと導くのでしょうか。
こうした疑問に対し、驚くほど精緻な答えを導き出した研究チームがあります。現在、順天堂大学に所属する金光昌史先生が主要メンバーの一人として在籍していた畠山昌則先生の研究チーム(現・微生物化学研究所)は、ピロリ菌が細胞に送り込む「がん化の実行犯」とも言えるタンパク質の実態を突き止め、たった一つのアミノ酸の違いが、地域による発がんリスクの差を生み出すという衝撃的なメカニズムを解き明かしてきました。本記事では金光先生へのインタビューを通して、壮大な疫学的謎が分子の言葉で語られるまでの発見の軌跡に迫ります。
未知への挑戦:ピロリ菌の胃がんへの関与が明らかになった日
── 金光先生がピロリ菌というテーマに惹きつけられ、研究の道に進まれたきっかけからお聞かせいただけますか?
金光: ここで「大学入学前からピロリ菌の勉強を独学で進めていて……」というストーリーがお話しできればスマートなのですが(笑)、私の場合は違いました。私は化学と生物学がもともと得意だったので、その流れで北海道大学理学部(化学科)に進学しました。そこで医学部・遺伝子病制御研究所の畠山昌則先生の講義を聞く機会がありました。これが間違いなく(人生の)大きな転機で、先生が講義で語られた「がんという疾患を、分子と分子が織りなす化学反応の集合体として紐解くことで、その発生をコントロールでき、完治も夢ではなくなる」というビジョンに、大きな衝撃を受けました。化学や分子生物学の発想で医学の難治性疾患を制御する、という未来に強く惹かれ、直ちに先生の研究室の門を叩きました。そこで行われていたのが、今では胃がんの原因と認識されるピロリ菌の発がん研究でした。
── 先生が研究を始められた2003年頃、ピロリ菌と胃がんの関係性はどのように理解されていたのでしょうか。
金光: 当時、胃がんは正常な胃から生じた炎症(胃炎)、胃の内壁に穴が開く胃潰瘍へと進み、その後、胃がんになるというように多段階的なプロセスで発生すると考えられていました。塩分の過剰摂取やストレスが胃炎や胃潰瘍の原因と言われていた一方で、1982年、オーストラリアのロビン・ウォレン、バリー・マーシャル両博士がピロリ菌が胃炎・胃潰瘍の原因になることを突き止めました。この成果に対し、2005年のノーベル医学・生理学賞が贈られています。
ただ、胃炎と胃潰瘍まではピロリ菌の感染が原因だということは社会的に認知され始めましたが、胃がんとの因果関係については懐疑的な見方も根強くありました。そんな中、呉共済病院で研究しておられた上村直実先生が、2001年に大規模な調査研究を発表されます。それによれば、約1500人の患者さんを8年間にわたって追跡した結果、胃がんを発症したのはピロリ菌に感染している人たちのグループだけだったのです。このデータは、ピロリ菌の感染が胃がんの発症に明確な因果関係を持つ可能性を示唆するセンセーショナルなものでした。畠山先生はピロリ菌の胃がんへの関与を示唆する他の多くの知見を統合し、その背後に存在するピロリ菌がヒトの胃にがんを発症させるメカニズムを分子レベルで明らかにしようと考えました。
──畠山研究室のチームが採用したアプローチには、どのような独自性があったのでしょうか?
金光:ピロリ菌は大きく分けて2種類あります。cagA(キャグエー)という遺伝子を持つピロリ菌と、持たないピロリ菌です。特にcagA遺伝子を持つピロリ菌は病原性が高いことがわかり、cagA遺伝子からつくられるピロリ菌のCagAタンパク質こそが発がんの「実行犯」ではないかと考えられるようになっていました。ただ、当時のピロリ菌研究の主流は、ピロリ菌そのものを培養細胞や実験動物に感染させる「細菌学的実験手法」を用いていました。この王道的な方法は、ピロリ菌が持つ多くの病原性の総和を観察できるメリットがある一方で、CagA以外のさまざまな因子が影響し合った観察結果が得られるため、CagA分子の純粋な機能を容易に見極めるには困難でした。そこで、もともと発がんを専門とするがん研究者だった畠山先生は他のチームとは全く異なるアプローチでピロリ菌/CagA研究に参入しました。「分子腫瘍学的実験手法」を軸としたCagA研究です。cagA遺伝子の配列を持つDNAを人工的に合成し、培養したヒトの胃の上皮細胞内に直接導入して、ヒトの胃の細胞内にCagAタンパク質のみを発現する「がん原遺伝子ハンティング」と同様の戦略です。「ヒトの胃の細胞にCagAが存在することで何が起き、その結果、胃の細胞はどのように変化するのか?」という未知の問いに対して、その答えを直接的に明らかにすることができると考えました。この独自の研究設計が、後に続く多くの発見の扉を開くことになります。
ミクロの攻防:たった一つのアミノ酸の違いが発がんリスクを分ける分子メカニズム
── 研究チームの革新的なアプローチは、「相関」の証明から、「因果」の分子メカニズムを解明する研究へと飛躍させたといえそうです。この独自の手法から、どのような発見につながったのでしょうか?
金光:最初の大きなブレークスルーは、CagAタンパク質がヒトの細胞内で「SHP2(シップツー)」というタンパク質と結合する発見をしたことです。
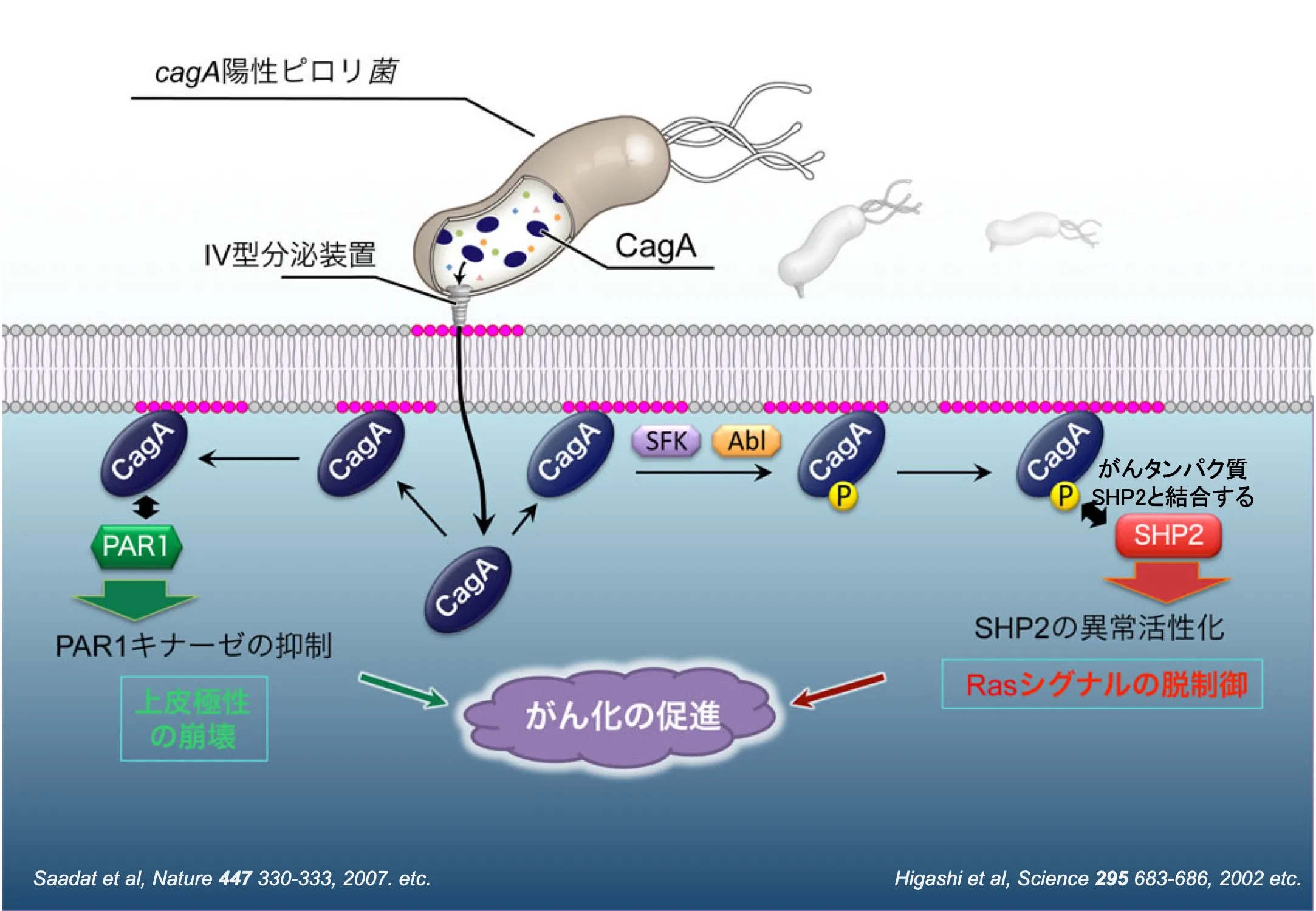
ピロリ菌は菌体の表面に「IV型分泌装置」と呼ばれる、ミクロの注射針のような巨大な多分子集合体を持ちます。ピロリ菌はこのミクロ針を感染したヒトの胃の上皮細胞に突き刺し、CagAタンパク質を直接、胃の上皮細胞の内部へと送り込みます。胃上皮細胞内に入り込んだCagAは、ヒトの細胞がもともと持っている酵素をハイジャックして「リン酸化」という化学的な修飾を受けます。[図中のP]このリン酸化修飾が、いわば「なりすまし」のスイッチとなります。リン酸化されたCagAは、あたかも以前からそこにあったヒトの細胞の情報伝達分子のように振る舞うことで、胃上皮細胞内の正常な生命活動を支える分子と次々に結合し、シグナル伝達回路を細胞内部からハッキングしその秩序を乱していくのです。[図1]
私たちは、CagAタンパク質が受けるリン酸化修飾がCagAを構成するアミノ酸のうち、チロシン残基に生じていることに注目しました。チロシンのリン酸化は、細胞分裂を必要とした細胞が、細胞内部へと増殖シグナルを伝達する過程で、増殖シグナルを伝えるバトンのような役割を持ちます。正常細胞ではチロシンのリン酸化程度やON/OFFのきりかえが厳密に制御されているのに対して、がん細胞では無秩序なチロシンリン酸化が生じており、その結果、制御を逸脱した形で細胞増殖が繰り返されることが知られていました。胃上皮細胞の解析を進めていくと、CagAのリン酸化されたチロシン部分に特異的に結合するヒトのタンパク質があることがわかりました。それが、SHP2という酵素でした。細胞増殖のアクセルを増強する分子で、白血病などの血液がんで異常活性化が見られる「がん原遺伝子産物」です。CagAタンパク質と結合すると、SHP2の酵素活性が制御不能に上昇し、胃の上皮細胞に対して「増え続けろ」という増殖シグナルを送り続けることを突き止めました。増える必要のない細胞がどんどん増え続けることで腫瘍ができ、これが、胃がん発症への引き金となるのです。[図1 右]。
私は畠山先生がこの成果を2002年に『Science』に発表され、CagAの悪しき素性の一端が明らかにされた時期に研究室にジョインしました。以降、北海道大学と東京大学の畠山先生の教室では、入室時の想像を超えた多くの興奮を体験しました。
──CagA病原活性の分子レベルの解析をもとに、「なぜ東アジアには胃がんが多く発症するのか?」という大きな謎を、CagA病原活性の分子レベルの解析で、どのように紐解いたのでしょうか?
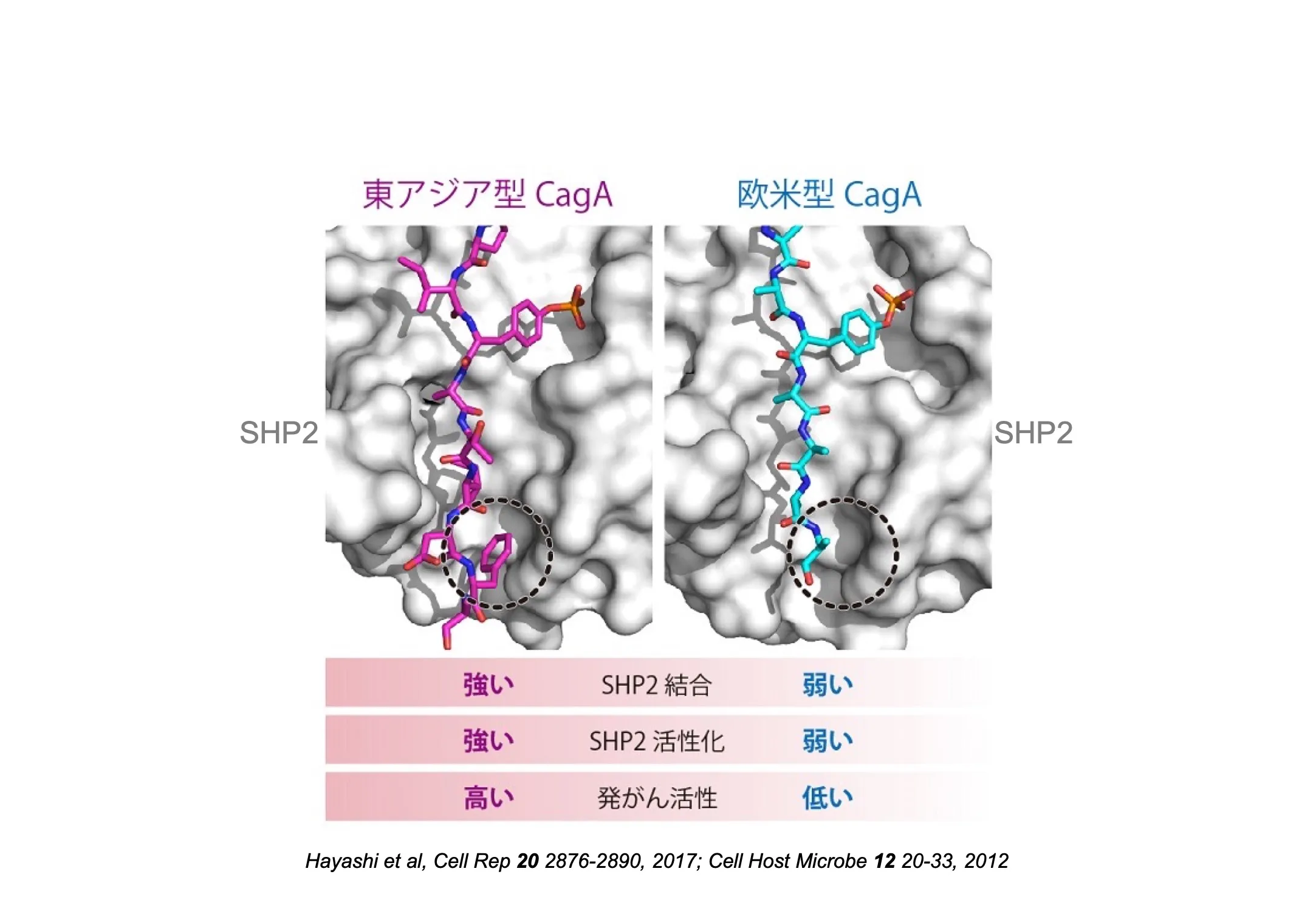
金光:まさにそこが次の焦点でした。世界の胃がんの発症率は、成人男性10万⼈あたり欧米では5〜8⼈であるのに対して、日本を含む東アジアでは約70⼈と歴然とした差があることは疫学的に知られていました。私たちは、この差がそれぞれの地域のピロリ菌がもつCagAの「型」の違いに起因するのではないかと考えました。研究を進めると驚くべき事実が判明しました。東アジアのピロリ菌が持つ「東アジア型CagA」と欧米のピロリ菌が持つ「欧米型CagA」とでは、先ほどお話ししたSHP2と結合する部位のアミノ酸の配列が、たった一つだけ異なっていたのです。このたった一つのアミノ酸の違いが、両CagAの機能に決定的な差を生み出していました。東アジア型のCagAは、欧米型に比べて約100倍の強さでSHP2と強力かつ安定的に結合することがわかったのです。鍵と鍵穴の関係に例えるなら、東アジア型CagAの「鍵(SHP2に結合する部分)」は、より深く、ガチっと「鍵穴(SHP2表面の溝)」にはまるのです。その結果、東アジア型CagAは、SHP2の酵素活性をより強く活性化し、細胞増殖シグナルをより強く異常活性化することがわかりました。[図2]
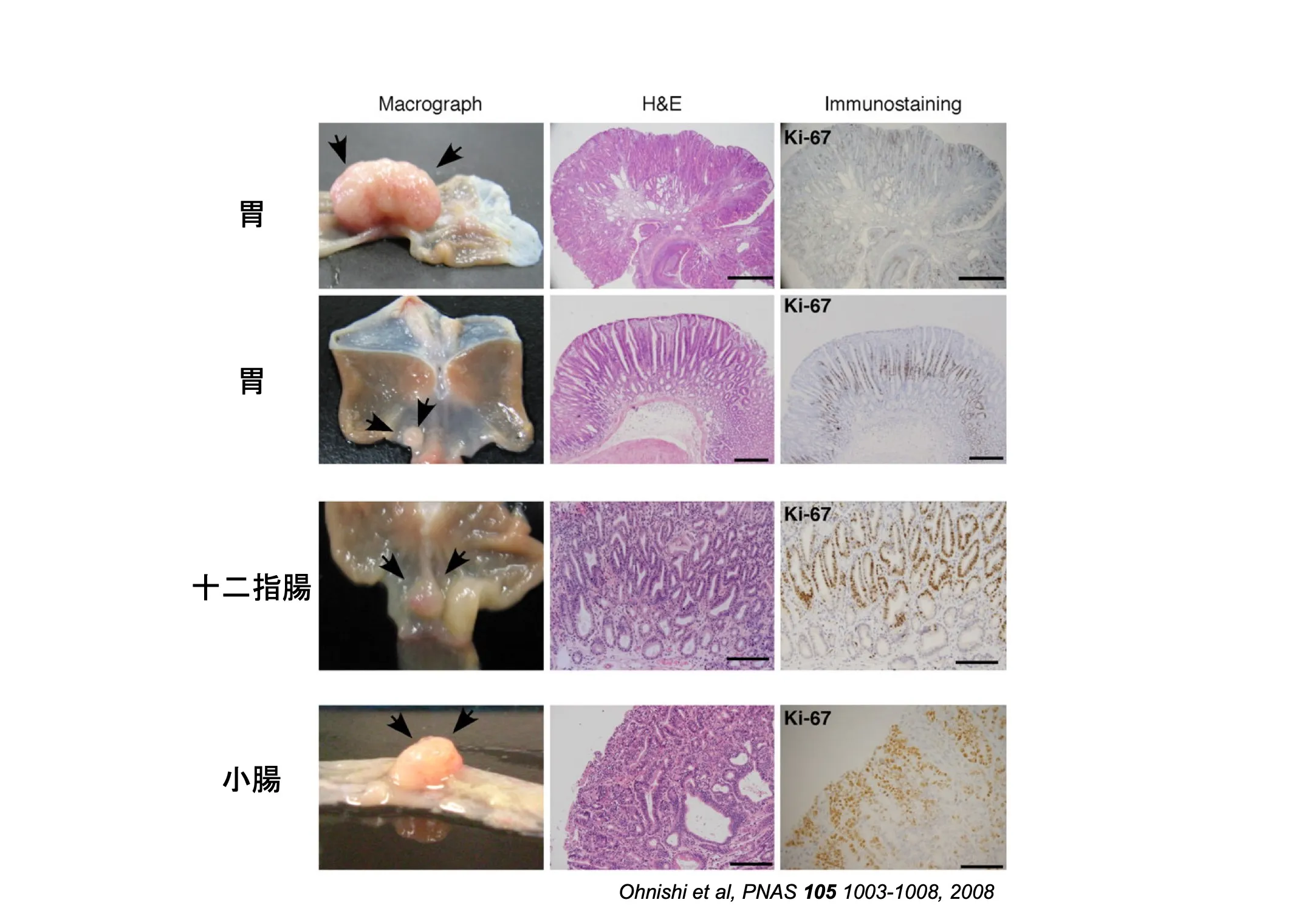
この結果が本当に発がん頻度の違いに繋がるのかを明らかにするために、私たちは2種類の遺伝子組み換えトランスジェニックマウスを作製しました。東アジア型CagAまたは欧米型CagAを全身の細胞で発現するcagAトランスジェニックマウスです。結果は衝撃的でした。どちらのcagAトランスジェニックマウスでも発がん剤などを投与せずとも消化器にがんを自然発症しました。さらに、東アジア型cagAマウスにおける発がん頻度は欧米型cagAマウスに比べて、約5倍以上でした。この結果は、欧米と東アジアの間に存在するヒト胃がん発生率の約10倍の違いを、両地域のCagAの配列差に着目して、マウス実験モデルで説明した成果となりました。CagAそのものが胃発がんリスクになり、さらに東アジア型と欧米型のSHP2結合部位のわずかなアミノ酸配列の違いが、哺乳動物の生体内でこれほど大きな発がん活性の差を生むことが、世界で初めて証明された瞬間でした。ピロリ菌はCagA以外の他の病原因子も多数もちますが、その中でも、まずは「CagAが単独で発がんを起こすことができるのか、白黒を付けよう」と、CagAにフォーカスし続けた畠山研究室のブレない信念の賜物なのだと考えています。[図3]
私たちは、SHP2の他にも、ヒト胃上皮細胞内でCagAが結合するヒトのタンパク質をいくつか発見してきました。その一つは、PAR1(パーワン)という、上皮細胞極性(細胞内の分子の位置どり)を制御して、細胞内の社会の秩序を守っている酵素です。ピロリ菌感染細胞では、CagAがPAR1と結合することで、PAR1の酵素活性が著しく阻害され、その結果、がん細胞で見られるように細胞内の分子配置の秩序が破壊されることを明らかにしました。この成果は2007年に『Nature』に掲載され、SHP2の脱制御とともに、CagAの発がん性を規定する胃上皮細胞内シグナルの二大攪乱として、以降のCagA研究の基盤となりました。[図1 左]
研究者の道:「Beginner’s Luck/Lack」に導かれた発見と、未来への展望
── 「CagAがVANGL(バングル)という分子を撹乱する」ことを最新の成果として発表されましたが、その裏には興味深いエピソードがあったと伺いました。
金光:はい。研究室員一丸で約20年間、ヒト胃上皮培養細胞、トランスジェニックマウス、胃のオルガノイドといった、正攻法とも言える実験試料を用いた解析を続け、CagAの撹乱標的分子/シグナルを多数同定してきました。一方で、多くを明らかにできたからこそ、ここからさらに未知のCagAの発がん促進活性を探索しようと考えると、誰もが行なっていない斬新な解析プロトコルに取り組む必要がありました。これがカエルを用いたチャレンジングなCagA実験の始まりでした。
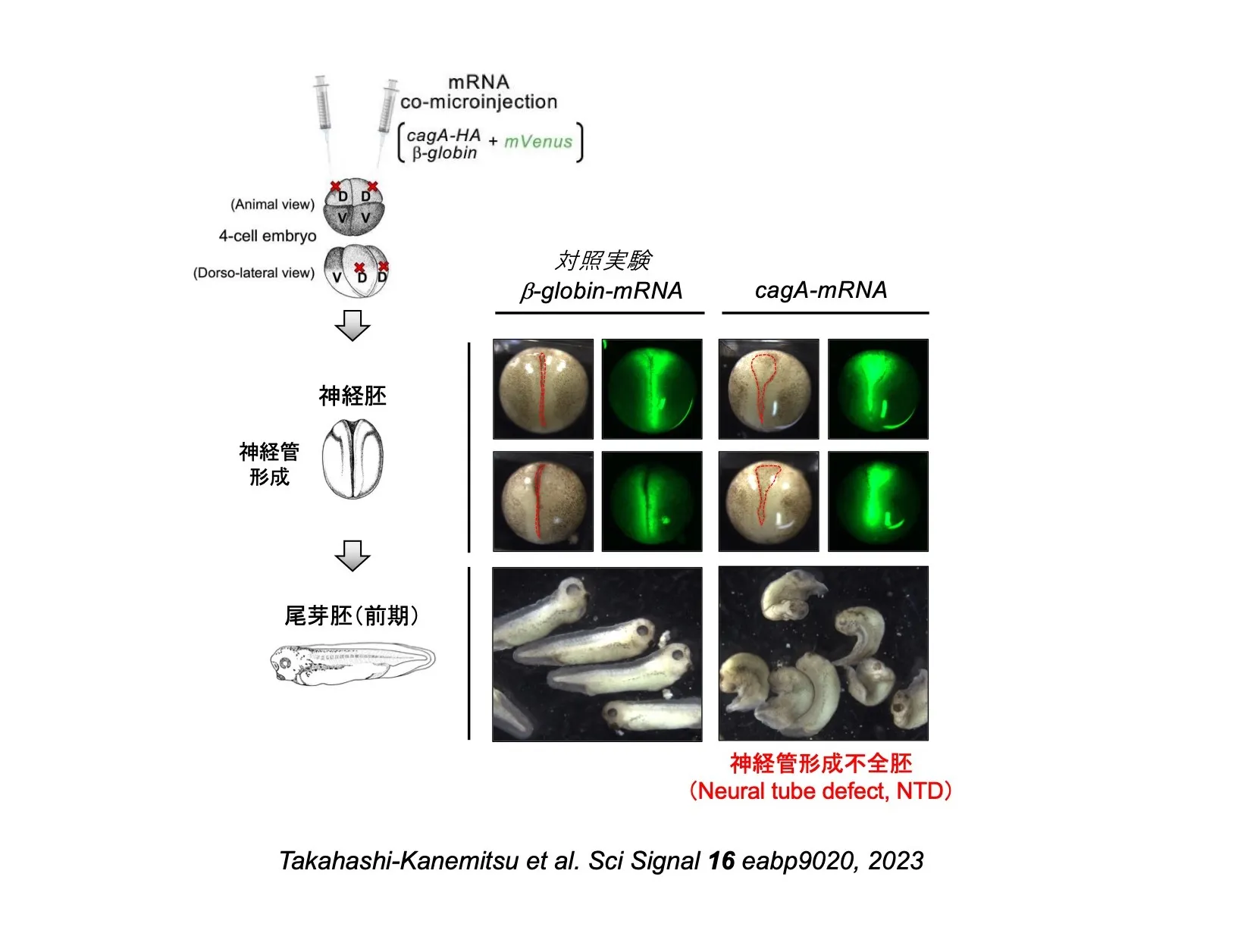
アフリカツメガエルは脊椎動物の胚発生の研究で最もよく用いられる実験動物の一つで、発生など生命維持に関わる多くの機構が哺乳動物との間で保存されています。受精卵から幼生(お玉杓子)が形作られていく過程で、個々の細胞が、どのタイミングで、どの遺伝子/シグナル経路を活性化して、どのように分裂・移動し、その結果どのような機能を持つ細胞に分化していくのか、細胞運命の系譜が分子レベルで理解されています。この利点を活かして、私たちは発生中のカエル胚にCagAを異所性に発現することで、形態形成の異常を引き起こし、その形態異常の特徴からCagAが機能を撹乱した脊椎動物細胞内の分子/シグナルを同定しようと発案しました。[図4]
実験に用いたカエル胚は、受精卵から2回の分裂を経た4個の細胞からなる初期胚で、腹側部を形作る運命を持つ濃い褐色の2個の腹側細胞と、背側部を形作る運命を持つ薄い褐色の2個の背側細胞から構成されています。[図4]当初の計画は、このうち2個の腹側細胞にcagAのmRNAを顕微注射することでした。腹側細胞は、ヒトの発がん研究で著名なβ-カテニンという分子の機能解析に適していることが発生学では既知だったからです。そこで、カエル胚実験の手解きを受け、濃褐色と判断した2個の腹側細胞を狙いcagA-mRNAを注射しましたが、cagA注射胚からβ-カテニンの機能異常を反映する既知の形態形成異常は生じませんでした。失意の中、結論の確証を得るために同じ実験を何度も繰り返しました。すると、cagAを注射した胚のうち1割程度で「頭尾の体軸が短くなり湾曲する異常(神経管形成不全)」が再現性良く生じることに気が付きました。この低頻度ながらもCagA発現胚で見られた形態形成異常は、試行回数の増加に伴うカエル胚実験の習熟に応じて発生率が低下し、やがてゼロになりました。これを実験系に不慣れな駆け出し期に得られた深掘りするに足りない実験結果と判断することもできましたが、私は「なぜ、この異常が『不慣れな』時にだけ『繰り返し』観察できたのか?」という問いを立てました。
その答えは、注射した細胞を追跡する目的でcagA-mRNAと一緒に注射していた蛍光トレーサー(venus-mRNA)の観察で明らかになりました。cagA-mRNAを注射され正常に発生したカエル胚は腹部にトレーサー蛍光が検出された一方で、cagA注射胚で形態形成異常を生じたものは背側にトレーサー蛍光が検出されました。胚によっては背/腹の褐色の濃淡が見分け困難なものがあり、特に不慣れで目利きが不正確な時には、背側細胞への誤注射が低頻度で起きていたことが分かりました。その後、背側細胞へのCagA発現を改めて行うと、ほぼ全てのカエル胚で神経管形成不全が生じました。この結果を手がかりにすることで、ヒトの先天性の神経管形成不全症で原因遺伝子として報告されるVANGLをCagAの標的候補分子としてピックアップすることができました。これを皮切りに、最終的にはCagAがヒトの胃上皮細胞内でVANGLと結合し、胃上皮幹細胞の運命決定を撹乱するというCagAの未知の発がん促進活性の発見につながったのです。[図4]
カエル胚を日常的に扱う発生学に精通した研究者であれば(あるいは高精度の画像認識AIで背腹を識別していたら)、100%の的中率で腹側細胞に遺伝子導入するため、この発見には至らなかったと考えられます。順天堂大学に異動後も関連データを積み上げ、着手から約8年を経て、この成果は『 Science Signaling 』の表紙論文として掲載され、また、日本ヘリコバクター学会学術賞などの受賞につながりました。今回、幸運にも「Beginner’s Luck/Lack」を発端として、想像を超える大きな結論が導かれることを経験し、「自分の期待とは異なる実験結果が得られた場合にも、そのデータに再現性があれば、落胆もほどほどにして深堀りしてみることが肝要である」という教訓を得ました。ペニシリン発見の経緯のように、これが歴史的な大発見に繋がったという事例も見聞きしますね(※)。
※1929年、イギリスの細菌学者A.フレミング(1881〜1955)がブドウ球菌を培養していた際に、偶然培養皿のなかにアオカビ(Penicillium notatum)が入り、そのカビの周りだけは細菌の発育阻止が生じていた。これに着目し研究を進めた結果、カビの中に菌の成育を抑える成分、ペニシリンが発見された。
── CagAの発がん研究で素晴らしい成果を上げられた後、現在は新たな研究課題に取り組んでいらっしゃるとのことですが、どのようなテーマでしょうか?
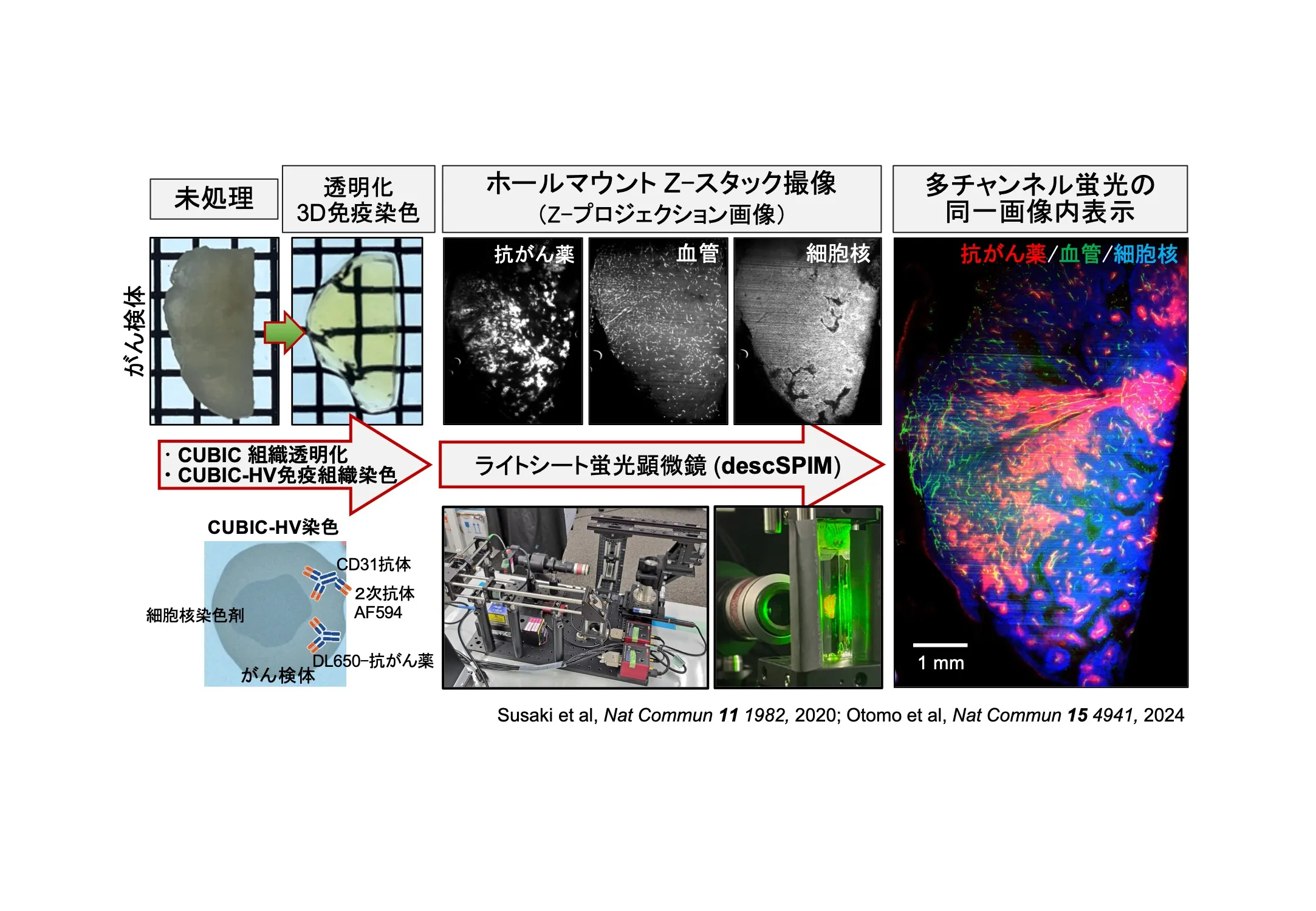
金光:現在は順天堂大学の洲﨑悦生先生の研究室で「CUBIC(キュービック)」と呼ばれる組織透明化技術を用いて、がんの3次元イメージングに取り組んでいます。これは、例えば、マウスから取り出したがんの塊を丸ごと特殊な試薬に漬けることで文字通りに「透明」にしてしまう技術です。この透明化技術を、組織染色剤や免疫染色抗体を組織検体の深部(表層から1 cmなど)に浸透させる独自技術「3次元組織染色」と組み合わせて使うと、例えば、「がんの中の、どこに・どのような種類の細胞や分子が分布しているのか?」、「投与した制がん薬はがんの中にどのように拡がるのか?」、「制がん薬が届きにくいがんの中の領域はどこなのか?」という謎に対して、がんの立体的な組織構造を保持したまま、全細胞を丸ごと見える化し、明らかにすることができます。例えば、血管の近傍に存在するにもかかわらず制がん薬が届いていないがんの中の微小領域があるとすると、その領域はがん再発の温床になると考えられます。そのような微小領域の場所と分子発現の特徴を網羅的に明らかにし、がん治療効果の向上を目指す研究を進めています。[図5]
これまで組織切片、すなわち「ある断面」での観察しかされてこなかったがんの塊を、ありのままに3次元で観察するプロセスは非常におもしろく、3次元で観察する以前には想定すら困難だった特異な組織構造や希少領域などを新たに発見して、純粋にワクワクしています。今後は、「分子腫瘍学」x「3次元組織イメージング」の掛け算から生まれる、3次元腫瘍組織学の開拓に尽力して行きたいと考えています。
「この人についていきたい」と心から尊敬できる指導者を見つけよう
── 先生のご経験を踏まえ、これから研究の道を選ぶ学生や若手の研究者に向けて、最も伝えたいアドバイスは何でしょうか?
金光:研究テーマそのものも重要であることは間違いないのですが、特に研究をスタートさせたばかりの学生さんや若手の研究者にとっては、「この人についていきたい」と心から尊敬できるロールモデルの研究者/指導者を見つけることがとても大切になります。研究を進める中で、目指す目標が高いほど、成果が出た時の興奮は大きくなりますが、同時に、困難や心労ならびに競合の度合いも必然的に大きくなります。そんなワクワクだけではない日々を乗り越えて前進し続けるためには、自分が目指すべきロールモデルが自分のできるだけ近くにいる環境が何よりも力になります。仮に、自分なりに調べた限り、その面白みや重要性に気が付けないような研究テーマが与えられたときにも、熟考のうえ、「この先生が夢中になって推すテーマなのだから、チャレンジしてみよう!」と一歩を踏み出す勇気をもらえるようなロールモデル指導者とチームを組むご縁をいただけたら最高ですね。
その上で、着眼点や手法のオリジナリティを武器に、他の誰にも真似できない競合優位性を持つ研究テーマに取り組むことも大切です。私は幸運にも、独自性の極めて高い2名のロールモデル研究者のもとで研究を進めるご縁をいただきました。畠山先生の細菌学的研究課題を「分子腫瘍学的視点から切り崩す」柔軟かつ独創的な方法論、そして洲﨑先生が世界に先駆けて開発された「CUBIC」透明化技術やその更なる有用改変は他の誰にも真似できません。誰と出会い、誰と一緒に取り組むか。その運やご縁のなかで培われた着眼点や手法が、結果としてオリジナルの研究テーマを生み出すための駆動力になると信じています。
金光(高橋) 昌史(かねみつ あつし)
順天堂大学大学院医学研究科 生化学・生体システム医科学、助教。北海道大学理学部(化学科)、同大学院、東京大学大学院医学系研究科にて、畠山昌則博士とピロリ菌CagAの発がん分子メカニズムの解明に取り組む(日本ヘリコバクター学会学術賞、Young Investigator Award, Japan-Korea Joint Symposium on Helicobacter Infection、 日本プロテインホスファターゼ研究会賞など)。2022年より現職で、洲﨑悦生博士のもとで組織透明化技術「CUBIC」を駆使し、がん組織の微小環境や制がん薬の腫瘍内分布などを3次元的に見える化する「がん組織の先端3次元イメージング」に取り組む。(がん関連三学会Rising Starネットワーキング優秀賞、車両競技公益資金記念財団 医療の基礎的先駆的研究に対する助成に採択など。)
※所属や肩書などはすべて掲載当時の情報です。
関連記事Recommend
-

【睡眠研究】人類に必要なのは冬眠…?冬に起きられない理由【動画で解説】
-

マウスからニワトリ、さらにターコイズキリフィッシュへ。生命の「時の設計図」解明のため、あえてモデル動物を変えていく荻沼チームリーダーの研究戦略
固定観念を覆すpH応答生物学の確立へ
-

尿からmiRNAを捕捉し、ステージ1からがんを早期発見。技術顧問としてのベンチャー共同創業
Craif株式会社 共同創業者・技術顧問 安井隆雄
-

独自のバイオインフォマティクス技術で、世界を変える酵素をデザインする
株式会社digzyme 代表取締役CEO 渡来 直生
-

スキンケアの疲労回復効果を検証!日常に取り入れる「疲労の科学」
~大阪公立大学健康科学イノベーションセンター~
-

「子どもたちを心臓の再手術から救いたい」――。思いを叶えるために根本教授が採ったユーザーイノベーション戦略
心・血管修復パッチ「シンフォリウム®」開発のキーマンに聞く「医師にしかできないサイエンス」とは
-

iPS細胞の実用化に向けた挑戦
京都大学iPS細胞研究財団
-

栄養学の新潮流「時間栄養学」とは? 私たちの健康を左右する、食事と体内時計の密接な関係に迫る!
-

次のパンデミックに備え、社会により貢献できる研究を目指して 慶應義塾大学医学部 感染症学教室 南宮 湖
臨床と研究をつなぎ国際保健に活かす「フィジシャン・サイエンティスト」を実践
-

CRISPR-Cas9の精度を飛躍的に高める「セイフガードgRNA」を開発した、九州大学川又助教の発想法