おもしろ実験や親子で楽しめる理系企画など、理系ゴコロをくすぐる情報が盛りだくさん。

私たちの生活の中には、「科学」で説明できることが多くあります。
見慣れている身の回りの自然を改めて科学的な視点で眺めてみると新しい発見や感動を知ることができます。毎日少しずつ変わる四季の変化から、いろんなサイエンスを親子で楽しんでみませんか。
アジサイの花は何色?
梅雨の時に美しく咲くアジサイの花は、日本の代表的な花のひとつです。アジサイは赤い花が咲いたり青い花が咲いたり、自在に花の色が変わることがあります。
これは簡単にいうと、アジサイが育っている土の状態によって赤色の花が咲いたり、花が青色になったりするのです。
アジサイを育てる人は、ピートモスや硫酸アルミニウムという物質を使って花を青くし、腐葉土や石灰を土に加えて赤い花になるよう工夫します。
近畿地方から中国地方にかけては花崗岩(かこうがん)で出来ている大地が多く、特に神戸の六甲山は花崗岩主体で出来ていることが知られています。花崗岩の土地に咲くアジサイは鮮やかな青色になることが多いと言われています※1。
アジサイの花の色はどうやって決まるのだろう?
アジサイの花の色はなぜ土によって変わるのでしょうか。
植物は一度発芽すると、場所を移動することができません。強い雨に打たれ、風に吹かれ、暑い日光にも冷たい雪にも耐えなければならないため、このような自然の変化から身を守る工夫をしています。
その工夫の一つに「アントシアニン※2」という色素があります。アントシアニンはポリフェノールの一種で、ブルーベリーや巨峰、なす、紫キャベツ、シソなどの食物にも含まれている色素です。アサガオやチューリップ、バラ、ハイビスカス、スミレなどの花にも含まれています。
アントシアニン色素は様々な環境の変化(温度、酸性度、濃度など)によって化学構造が多様に変化し、これらによっていろんな色に見えるようになります。
アジサイの花に含まれるアントシアニン色素は、土の「酸性度」が変わることによって、花の色が赤色や青色に自在に変化するのです。

アジサイが何色になるのか咲くまで待つのも楽しみだけど、土の酸性度を測って、事前に何色になるか調べることもできるよ。

へー、そうなんだ!

土以外にもいろいろな身の回りのモノの酸性度が調べられるよ。
「酸性」「中性」「アルカリ性」とpH(ぴーえいち)のおはなし
小学校の理科の実験でリトマス試験紙を使用したことはありませんか?青色リトマス紙と赤色リトマス紙があり、青色が赤く変わった時その水溶液を「酸性」といい、赤色リトマス紙が青く変化したら「アルカリ性」であると習ったのを覚えているでしょうか。
リトマス試験紙を使うと、水溶液の液性「酸性」「中性」「アルカリ性」を調べることができます。
「酸性」「中性」「アルカリ性」というのは水溶液の性質を表す指標のひとつで、水溶液の中に存在する水素イオン(H+)の量によって決まります。水素イオンの量(水素イオン濃度)によってもっと細かく溶液の特徴を表す指標にpH(ぴーえいち)というものがあります。※3
0から14の範囲で表し 、pHが7の時を「中性」、7よりも小さい時を「酸性」、7より大きい時を「アルカリ性」と呼んでいます。
pHを調べるにはpH試験紙やpH電極などいくつかの方法があります。
身近なもので「酸性」「中性」「アルカリ性」を調べよう
リトマスというのはリトマスゴケという菌類の一種から得られる色素です。この色素をろ紙にしみ込ませたものがリトマス試験紙と呼ばれているものです。
自然の中にはリトマスゴケのように酸性やアルカリ性によって色が変わる色素を持っているものがたくさんあります。私たちが普段から食べている食物の中にもいくつか見つけられます。これらの色素を利用して、「酸性」「中性」「アルカリ性」を調べることができます。
【準備するもの】
- 身近な植物のエタノール抽出液
Yumiはハーブティーに使われるハイビスカスとジャーマンカモミール、紅茶の葉、そしてお庭に咲いている紫蘭(シラン) の花を摘んできました。これらを無水エタノールに浸して室温で1日置くと色素が抽出されます。
- 10%クエン酸水溶液、10%炭酸水素ナトリウム水溶液の調製
次にクエン酸2gを水18gに溶かして「10%クエン酸水溶液」を調製しました。炭酸水素ナトリウム(重曹)2gも水18gに溶かして「10%炭酸水素ナトリウム水溶液」を調製しました。水道水(ミネラルウォーター、コンタクト用の精製水でもよい)を準備しました。
- pH試験紙(Advantech 社製、pH0-14、9 x 5.5mロールタイプ)
- 製氷皿(絵の具のパレットなどでも可)
Yumiは100円ショップで売られている製氷皿を利用しました。 - スポイト数本
【実験】
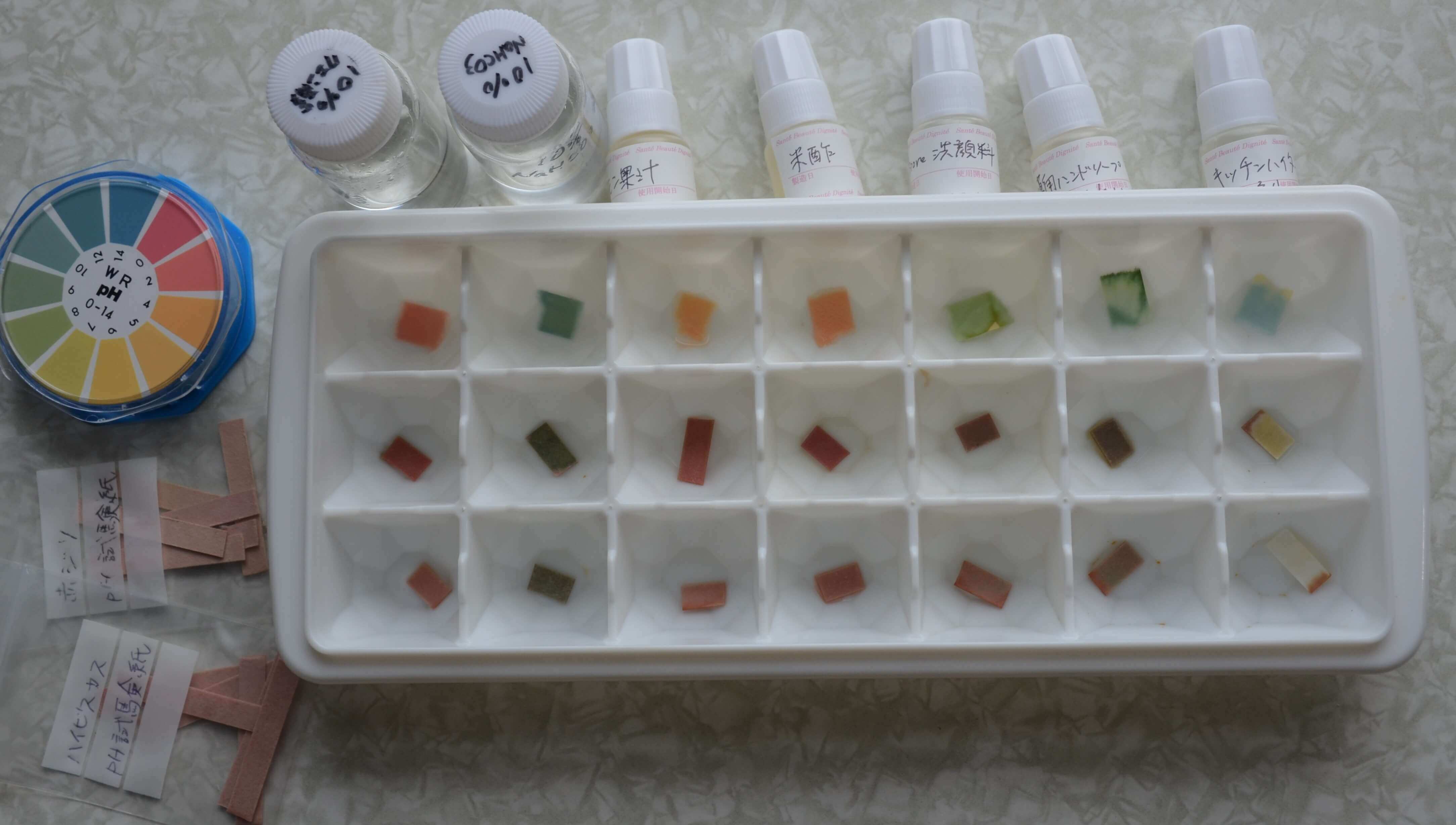
- クエン酸水溶液、水、炭酸水素ナトリウム水溶液を入れます。
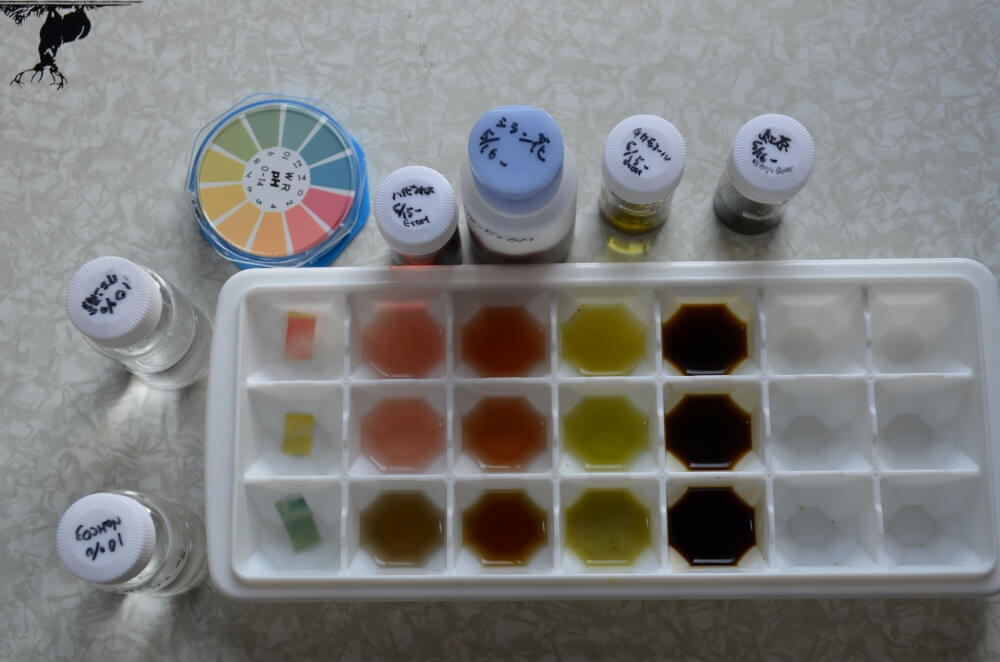
製氷皿を横に長い向きにして置き、一番上の一行に10%クエン酸水溶液を5区画、それぞれ1mLずつ入れます。同様に2行目には水を1mLずつ入れます。3行目には10%炭酸水素ナトリウム水溶液を1mLずつ入れます。クエン酸水溶液は「酸性」、水は「中性」、炭酸水素ナトリウム水溶液委はアルカリ性のサンプルとなります。 - pH試験紙で色を確かめてみよう。
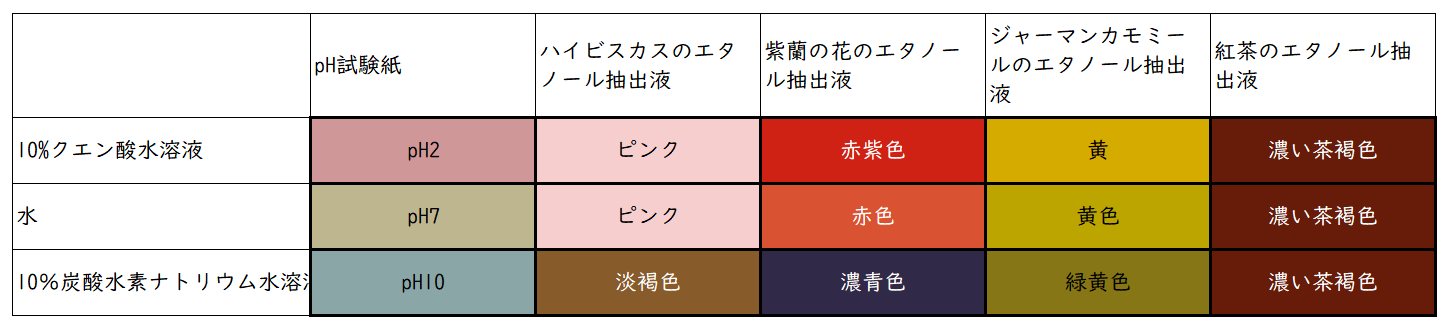
一番左の列の3つ(上:クエン酸水溶液、中:水、下:炭酸水素ナトリウム水溶液)にpH試験紙の断片を少しだけ浸してみて、色の変化を調べましょう。試験紙についている色見本と比べるとその水溶液のpHがわかります。写真の場合、10%クエン酸水溶液はpH2、水はpH7、10%炭酸水素ナトリウム水溶液はpH10だということがわかります。 - 植物の色素の色の変化を調べてみよう
左から2列目にハイビスカスの抽出液を2~3滴加えてみましょう。無水エタノールで抽出したハイビスカスの色素は真っ赤なきれいな色をしていますが、どんな色に変化するでしょうか。 -
クエン酸水溶液と水ではピンク色ですが、そのピンク色は同じではありませんね。炭酸水素ナトリウム水溶液では少し緑かかった茶色のような色にも見えます。Yumiなら淡褐色と表現しますが、みなさんはどんな色に見えるでしょうか。
同様に、紫蘭の花、ジャーマンカモミール、紅茶からの抽出液も加えて色の変化を調べてみましょう。これらの植物色素では、炭酸水素ナトリウム水溶液(アルカリ性)で色が大きく変化するものが多く見られました。
紅茶の色は一見同じように見えますが、炭酸水素ナトリウム水溶液の色は、クエン酸水溶液、水のものよりも少し濃くなっているように見えます。加える紅茶色素の量を少なくすれば、もっと色の差が見やすくなると考えられるので工夫してみてはいかがでしょうか。
10%クエン酸水溶液はpH2の酸性、水(水道水)はpH7の中性、そして10%炭酸水素ナトリウム水溶液はpH10のアルカリ性であることがわかります。
また、花や飲み物に使われる植物の色素の中にも酸性・中性・アルカリ性によって色が変わるものがあることがわかります。特に、アルカリ性で色が変化する色素が多いことがわかります。
つまり、pH試験紙やリトマス試験紙がなくても、身近な色素を利用すれば、酸性・中性・アルカリ性をおおざっぱに知ることができることがわかります。
クエン酸、炭酸水素ナトリウムの濃度を変えて色の変化を調べてみよう
10%クエン酸水溶液は酸性、10%炭酸水素ナトリウム水溶液はアルカリ性であることがわかりました。では、クエン酸や炭酸水素ナトリウムの濃度が違うと、酸性やアルカリ性の強さは異なるのでしょうか。濃度を変えて調べてみましょう。
【準備】
10%クエン酸水溶液を薄めて(希釈)、異なる濃度の水溶液を作りましょう(調製)。
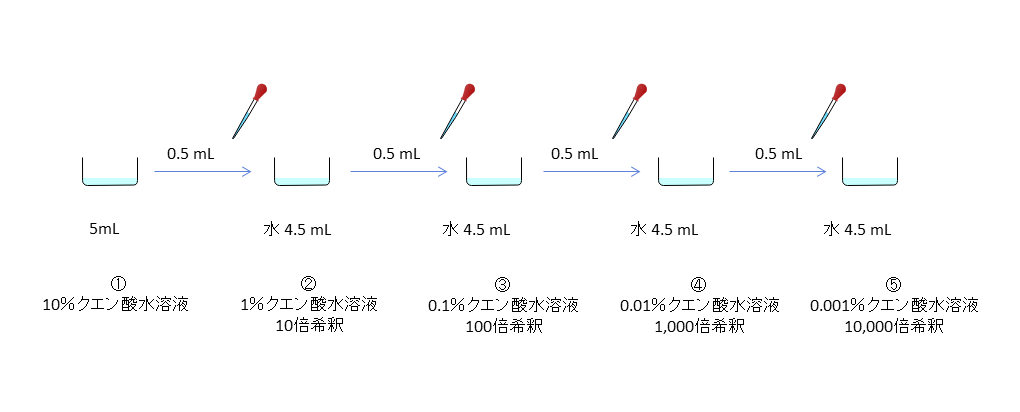
製氷トレイの一番左(①)に10%クエン酸水溶液を5mL入れます。①の右となり(②)に水を4.5mL入れ、①から0.5mlとって②に入れてよく混ぜます。②は10倍に希釈したことになるので、1%クエン酸水溶液が出来たことになります。
②の右となり(③)に水を4.5mL入れ、②から0.5 mLとって③に入れてよく混ぜます。③には②の10倍希釈された0.1%クエン酸水溶液が出来たことになります。
同様にして右側に④(0.01%)、⑤(0.001%)の希釈水溶液を作ります。
10%炭酸水素ナトリウム水溶液①についても同じように希釈して、1%、0.1%、0.01%、0.001%の水溶液を作りましょう。
【実験】
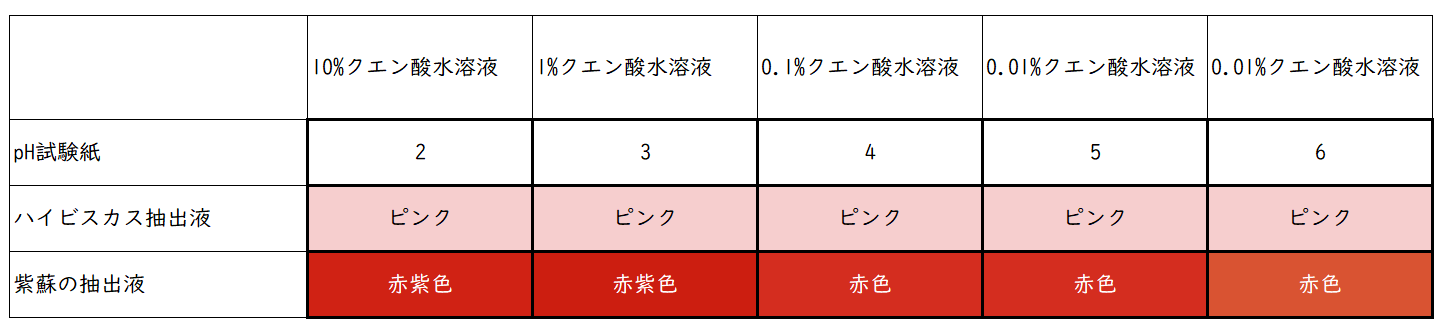
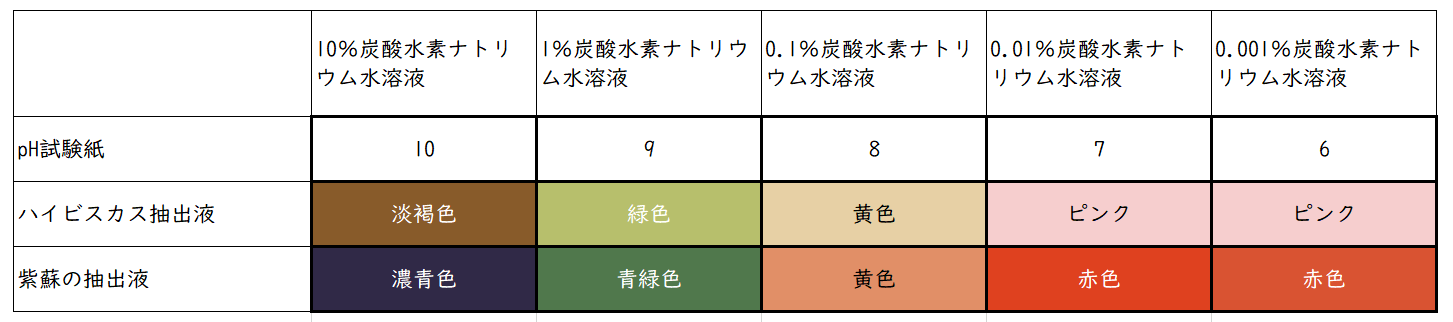
クエン酸水溶液と炭酸水素ナトリウム水溶液、合計10種類の水溶液についてpH試験紙でpHを調べてみましょう。また、ハイビスカスの色素を数滴加えて、色の変化を調べてみましょう。
紫蘇(シソ)の色素でも試してみましょう。
クエン酸水溶液は、濃度が10分の1になるとpHが1大きくなっています。炭酸水素ナトリウム水溶液は濃度が10分の1になるとpHが1小さくなっています。そしてどちらの場合も中性(pH7)に近づいています。
つまり濃度が10倍薄くなるとpHが1変化し、中性に近づいていくことがわかります。
ハイビスカスや紫蘇など酸性とアルカリ性で色の違いが大きかった色素では、クエン酸や炭酸水素ナトリウムの濃度の違いによっても色が変わることがわかります。特に中性からアルカリ性側(pH>7)での色の変化がはっきりしています。ハイビスカスよりも紫蘇の方が色の変化する領域が広く、pHを調べるのに利用できることがわかります。
身近なものでオリジナルの試験紙を作ろう
身近な色素を使って、オリジナルのリトマス試験紙を作ってみましょう。ここではハイビスカスと紫蘇を使ってみました。
【準備】
- ハーブティー用ハイビスカス
- 青紫蘇(梅干し用、紫蘇ジュース用、乾燥したふりかけなど)
- 無水エタノール
- 試香紙(画用紙、ケント紙、ろ紙などでも可)
【作り方】
ハーブティー用のハイビスカスを無水エタノールに浸して一晩置きます。青紫蘇を無水エタノールに浸して一晩置いておきます。着色したエタノール溶液を別の容器に入れ、ここに3~4㎝の長さに細く切った紙を浸します。翌日に取り出してよく乾燥させます。
【注意】
色素を吸収した紙を乾燥させるときは、網などを使ってできるだけ接着面を少なくするときれいに色素が残ります。出来たオリジナル試験紙は長時間保存すると色が薄くなってくるものがあります。出来るだけ早く使いましょう。
身近なものの酸性・中性・アルカリ性を調べよう
家の中にはいろんな水溶液があります。食卓、台所、洗面所、浴室などにあるいろんな水溶液を探して、作った試験紙で色の変化を調べてみましょう。
Yumiはお家の中から、レモン果汁、米酢、洗顔フォーム、薬用ハンドソープ、洗濯用の漂白剤を選んできました。pH試験紙、紫蘇の試験紙、ハイビスカスの試験紙に、これらを1滴しみこませて色の変化を調べてみましょう。
(注意!)これらの水溶液の中には、目や口に入れると危険なものもあります。特に漂白剤は絶対目や口に入れないようにし、手についたらすぐに大量の水道水で洗ってください。
これらの結果からどんなことが考えられるでしょうか。
レモン果汁にはクエン酸という酸性の化合物が含まれています。米酢(お酢)には酢酸という酸性の化合物がおおよそ4%含まれています。この2つはどの試験紙も酸性を示しました。
洗顔フォームは顔を洗う時に使うせっけんで、ハンドソープは手を洗う時に使うせっけんです。せっけんは弱酸性の体の汚れを落とすのでアルカリ性のものが多く用いられています。これらのせっけんもアルカリ性を示しています。
漂白剤は「水酸化ナトリウム」という強アルカリ化合物を水に溶かしたものです。さらに次亜塩素酸ナトリウムという化合物も含まれています。試験紙はすぐに鮮やかな青色になりますが、次亜塩素酸ナトリウムの影響によりすぐに色が消えてしまいます。特にハイビスカス試験紙はあっという間に真っ白になってしまいます。
他にも、しょうゆ、オレンジジュース、コカ・コーラ、温泉水、川の水など身近な水の酸性・アルカリ性を調べてみましょう。
身近なものの酸性・中性・アルカリ性から環境を考えよう
身近なものには、酸性を示す水溶液とアルカリ性を示す水溶液があることがわかりました。
川や池で魚や水草が元気に暮らすには、その水は中性付近であることが大切です。そのため、私たちが流した生活排水は自然を破壊することのないように処理されてから川や海に流されます。
日本では法律によって河川に捨てる水のpHは5.8~8.6、海へはpH 5~9でなければなりません※4。
①残ったお酢を川へ捨てちゃったら?
お料理で使わなかった期限切れのお酢(500mL)があったとします。お酢はpH3の酸性ですから、川にザザ~っと捨てるにはpH6くらいにしなければなりません。10倍に希釈するとpHが1大きくなるので、4500mLの水でうすめるとpH4になります。pH6にするにはさらに10 x 10 = 100倍希釈しなければなりません。
すなわち、たった500 mLのお酢を川に捨てるには、1000倍に薄めなければいけないことがわかります。必要なお水の量はおおよそ500リットル!お風呂2杯分くらいのお水といっしょに流さないと、お魚の住めない水になってしまうということになります。
漂白剤はpH14という大変強いアルカリ性です。pH9にするには10 x10 x 10 x 10 x 10 = 100,000、つまり10万倍に薄めなければいけないことがわかります。
みなさんが大好きなオレンジジュース、コカ・コーラなど、身近には酸性の飲み物が多くあります。何気なく道端にポイっと捨ててしまうと、自然環境に大きな影響を与えてしまうことになります。
②楽しい源泉かけ流し温泉、その後は?
日本には「温泉」という入浴文化があります。日本各地にはいろんな色やかおり、健康に効果のある温泉があります。
群馬県にある草津温泉は、日本を代表する温泉のひとつです。草津温泉街の中心には「湯畑(ゆばたけ)」と呼ばれる場所があります。ここには湯畑源泉という温泉がわき出しています。この温泉水は腐った卵のような強い臭いがあり、お湯はpH2.0という強い酸性を示しています※5。湧き出すお湯の量が豊富なので、多くの温泉旅館では温泉水をそのままお風呂に使った「源泉かけ流し」を行っています。
みんなが楽しんだpH2の酸性のお湯はそのまま捨てるわけにはいきません。草津温泉では温泉水を処理する設備を持っていて、ここで中和剤を加えてpH7付近にしてから川へ放流しているのです。私たちの健康づくりに役立つ温泉は、川の生き物や植物にとっては毒水でしかありません。捨てる前には自然を守る工夫が必要なのです。
さらに詳しく知りたい方へ
※1
花崗岩由来の地質には炭酸イオンや硫酸イオンなどが多く含まれているため、酸性に偏る傾向があると言われています。酸性土壌の場合はアジサイの花は青く、アルカリ性土壌の場合は赤くなると言われますが、実際にはアルミニウムイオンも発色に関与しています。品種によっては色が変化せず、どんな土壌でも赤い花が咲いたりする品種もあります。ちなみに、アジサイが初めて発見されたのは神戸六甲山で、シーボルトが見つけたシチダンカだと言われています。参照)村松邦彦著「花づくり大百科」、主婦の友社(1991年)
※2
アントシアニン(Anthocyanin)はギリシャ語から派生した言葉で、anthos(花)とcyanos(青)に由来しているとされています。天然由来のアントシアニン化合物は非常に多く、現在知られている代表的なものだけでも500以上あると言われています。これらのアントシアニン化合物は、酸性度(pH)や温度、濃度、共存する金属イオンや酵素などの他の化合物などの条件によって少しずつ化学構造が変化し、これによって吸収する光の波長が変わることにより、赤紫~青紫の色調に発色することが知られています。
参照)山田洋一ら著「アントシアニン系色素における呈色の経時変化」、宇都宮大学教育学部研究紀要第66号第2部別冊(2016年)
※3
私たちの周りにある物質はすべて化学物質から出来ていますが、化学物質をされに細かい単位に分けていくと分子となりさらに原子になります。原子の中には、電気を帯びているものがあり、プラス(+)側に偏っているものを陽イオン、マイナス(-)側に偏っているものを陰イオンと呼んでいます。水溶液中にある水素イオンの濃度から計算されるものに「水素イオン指数、pH=ピーエイチ」という物理量があります。
pH = -log[H+]
というのが定義で、「log」というのは常用対数と呼ばれるものです。[H+]は水素イオン濃度のことを表しています。
例えば10 x 10 = 100ですが、10を2回かけることを「102(10の二乗)」と書き、
log 100 = log 102 = 2
と書きます。
また、0.1 x 0.1 = 0.01 であり、0.1(1/10)を2回かけることを「10-2(10のマイナス二乗)」と書き、
log 0.01 = log 10-2= -2
となります。
つまり、「10を何回かけるとその数字になりますか?」というのが「log」の意味になります。
pHという観点でいうと、水素イオンが1L中に0.01モル(0.01g)含まれていると、
-log[0.01] = 2
となり、
pH =2
ということになります。
同様に計算すると、水素イオン濃度が0.001(0.01 x 0.1)の場合は、pH = 3となります。水素イオン濃度が10倍薄くなるとpH値が1大きくなります。
常用対数というのは高校数学の教育項目になっています。
参照)
神谷功ら著「図説 化学の基礎」10章・水素イオン濃度とpH、p54-55、東京教育社(1988年)
分析化学研究会編著「定量分析・改訂版」第4章・中和滴定、p74、廣川書店(1991年)※4
環境省が定める一般排水基準の中に水素イオン濃度(水素指数、pH)に関する基準値が示されています。これによると、「海域以外の公共用水域に排出されるもの」はpH 5.8以上8.6以下、海域に排出されるものはpH5.0以上9.0以下でなければならないと定められています。これらのpHの試験法は JIS K 0101,JIS K 0102及びJIS B 8224によって定められており、正しく校正されたガラス電極法を用いた値を採用することになっています。※5
草津温泉湯畑源泉は、白幡源泉と並んで草津温泉の中でも古い源泉のひとつです。その泉質は「酸性・含硫黄―アルミニウムー硫酸塩・塩化物泉」という名前がついています。水素イオンは8.91 mg/L含まれ、硫酸イオン640 mg/L、ヒドロ硫酸イオン 192 mg/Lも含まれている典型的な硫酸酸性の湯です。特有の腐卵臭は、遊離硫化水素7.1 mg/Lによるものです。豊富な量のメタケイ酸216 mg/Lにアルミニウムやマンガン、鉄などの金属イオンが含まれ、微妙な緑や青色が見える白濁した魅力的なお湯となっています。
草津の湯はその溶存成分と強酸性の泉質ゆえに皮膚病に効果が高いと言われ、「時間湯」という特殊な入浴方法での湯治が行われてきました。郊外には感染病の治療施設が作られたこともありました。
なお、強酸性の温泉では、石けんの泡立ちが悪くなる傾向にあります。目などの粘膜に触れると刺激があるので、酸性の湯では洗顔や洗髪は避け、切り傷のある時は入浴は避けた方がよいと言われています。
参照)
遠間和広著「温泉ソムリエテキスト」、三条印刷株式会社(2015年)
関連記事Recommend
-

親子で楽しもう、身の回りのサイエンス
第11話「湿度を測ろう」中学生向け
-

親子で楽しもう、身の回りのサイエンス
第10話「雲を観察しよう(後編) ~季節によって変わる雲~」
-

親子で楽しもう、身の回りのサイエンス
第9話「雲を観察しよう」前編
-

【保存版】夏休みの自由研究に!動画と文でわかる! 簡単だけどちゃんと科学できる実験25選
-

自由研究にオススメ!平均15分で終わるおもしろ科学実験5選【小学生〜中学生向け】
-

親子で楽しもう、身の回りのサイエンス
第8話「天気図を書こう」
-

親子で楽しもう、身の回りのサイエンス
第7話「植物のかおりをとりだしてみよう」
-

親子で楽しもう、身の回りのサイエンス
第6話「植物の色素で染めてみよう」
-

親子で楽しもう、身の回りのサイエンス
第4話「色を分けてみよう」
-

最短5分!手軽にできるおもしろ科学実験10選(後編)夏休み自由研究にもオススメ!