幹細胞(stem cell)とは
私たちの体を形作る細胞には寿命があり、とくに皮膚や血液のような細胞は寿命が短いため、絶えず新たな細胞を生み出して補充する必要があります。その役割を担う細胞が「幹細胞」です。幹細胞から生み出された細胞は、機能の異なる様々な細胞に変化(分化)します。そして傷ついたり、古くなったりした細胞と入れ替わることで生体が維持されています。
プラナリアという生物をご存じでしょうか?川などに生息している体長1〜3cmほどの原始的な無脊椎動物(背骨を持たない動物)の一種ですが、全身に幹細胞が分布しており、無性生殖において自分自身を切断したあと、脳や目を含めて完全に個体として再生します(人工的に切断しても再生します)。プラナリアほどではないにしろ、ヒトを含め動物は、幹細胞のおかげで傷ついたり失われたりした細胞を再生し、生体を維持することができているのです。
幹細胞の2つの特徴
幹細胞を定義づける2つの重要な特徴があります。1つ目が、自分と同じ能力を持った細胞に分裂することができるというもので、これを「自己複製能」と呼びます。この能力のおかげで、幹細胞はほぼ無限に新しい細胞を生み出すことが可能となっています。二つ目の特徴は「分化能」です。分化とは、受精卵が細胞分裂を繰り返しながら増殖し、神経や臓器、筋など、それぞれの機能と役割を持った個々の細胞に変化していくことを言います。通常、分化が決定した細胞(体細胞)は、他の細胞にはなれません。つまり幹細胞は、細胞が個々の役割に細分化される前段階の細胞ということになります。
この幹細胞の特徴を利用して、人工的に組織・臓器を再生する試みや、細胞を体内に移植し患部に作用する治療法(再生・細胞医薬品)の開発が近年盛んに試みられています。これまで治療法のなかった多くの疾患への応用が期待されているため、幹細胞に関わる研究者に対して、複数のノーベル賞が授与されています。iPS細胞を作り出した京都大学の山中伸弥教授はあまりにも有名ですね。
医療応用だけでなく、幹細胞そのものを研究することも重要です。発生の過程や疾患に至る過程などの解明が進み、生命科学の基礎研究においても大きな進展が期待できます。
幹細胞の種類(体の中の幹細胞)
私たちの体は数十兆個の細胞からできています。細胞分裂を繰り返すことで作り出されたこれらの細胞(体細胞)は、さかのぼると全て1つの受精卵にたどりつきます。受精卵は高等生物において1個の細胞から個体を作り出せる全能性を持った幹細胞です。(全能性:あらゆる細胞に分化し完全な一個体を形成できる能力)
分裂を繰り返した受精卵は均一な細胞の集団から、不均一な細胞の集団へと変化し「胚」になります。初期の胚の中では体や生殖細胞を作るもととなる幹細胞が、他の細胞から分かれて細胞塊を形成していきます。細胞塊では将来どの細胞に分化していくかの運命が決まっていきます。この初期の胚の細胞塊から細胞を外部に取り出して培養したものをES細胞(Embryonic Stem Cell)と呼びます。ES細胞は体内に存在する全ての細胞に分化することができます(これを「多能性」と言います) 胚の一部から取り出した幹細胞のため、胚性幹細胞と呼びます。
一方で、すでに個体として分化が進んだ生体の中にも幹細胞が存在しています。体のさまざまな場所に存在し、各部位の細胞の修復再生を司っています。これらの幹細胞を総称して組織幹細胞と呼びます。組織幹細胞が分化できるのは細胞が存在する場所に関連する細胞だけです。例えば、造血幹細胞は骨髄にあり、赤血球や白血球などの血液細胞を作ります。また肝臓幹細胞は肝臓の細胞を作り、神経幹細胞は神経細胞を作ります。組織幹細胞の全貌はまだ明らかになっておらず、新たな組織幹細胞の発見が報告され続けています。
<幹細胞は大きく二つに分けられる>
胚性幹細胞(ES細胞)
・受精卵が数回分裂した胚から取り出され培養できるようにした細胞
・体内に存在する全ての細胞に分化することができる
組織幹細胞
・体内の組織中に存在する幹細胞
・存在する場所に関連する細胞にのみ分化する
例) 上皮幹細胞、骨格筋細胞、心筋細胞など
多能性を持つES細胞とiPS細胞は人工的に作られる
ES細胞のように、体を構成する全ての細胞に分化できる幹細胞を多能性幹細胞(PSC: Pluripotent Stem Cell)と呼びます。山中伸弥教授らが樹立したiPS細胞もPSCです。両者ともに人工的な操作を施し得られます。この技術を得たことは、生命科学の基礎研究はもちろんのこと医療にも大きな可能性をもたらす大変なブレークスルーでした。以下、ES細胞とiPS細胞という2つのPSCのそれぞれの発見の経緯と特徴を紹介します。
<ES細胞>
初期胚から細胞を取り出し培養するES細胞は、1981年にイギリスのエヴァンス(Martin J.Evans)によりマウスの胚から初めて樹立されました。あらゆる細胞に分化できる細胞の培養に成功し、この功績により後にノーベル賞を受賞します。1998年にはアメリカのトムソン(James A. Thomson)が人工授精の余剰胚からヒトのES細胞の樹立にも成功します。ヒトES細胞は再生・細胞医療における重要な細胞として大きな期待が寄せられました。どんな細胞にも分化できほぼ無限に増殖するため、組織を再生して移植したり、細胞が関わる疾患(白血病など)の治療に役立てることができると考えられたのです。
一方で、ES細胞には2つの大きな課題がありました。1つ目の課題は移植する際に生じる拒絶反応です。ES細胞は、他人の受精卵から作る必要があります。そのため一般的な臓器移植と同様に他人の細胞に対する拒絶反応が発生します。
もう1つの課題は倫理的なものです。ES細胞はその作製過程で生命の源である胚の破壊を伴います。そのためES細胞の研究に対して、各国でさまざまな規制が設けられています。ヒトES細胞を最初に樹立した米国では、当初多くの資金が出されていましたが、ブッシュ大統領の時代(在任: 2001年 - 2009年)に制限されます。その後、オバマ大統領(在任:2009年 - 2017年)の声明で制限は撤廃されましたが、2020年に新設された倫理諮問委員会で、ほぼすべてのヒトES細胞研究の申請が不許可になるなど慎重な議論が続いています。日本ではヒトES細胞の研究は長年禁止されていました。最近少しずつ規制が緩和される方向にありますが、海外と合わせ今後の動向を注視する必要があるでしょう。
<iPS細胞>
ES細胞の課題への議論が進められる中、全く異なる方法でPSCが生み出されました。それが、2006年に京都大学の山中伸弥教授らにより発表されたiPS細胞(人工多能性幹細胞:induced Pluripotent Stem Cell)です。
山中教授らは、すでに分化した細胞を、受精卵のような分化能力を持つ状態に戻す方法(初期化、リプログラミングともいう)を探っていました。注目したのはES細胞や生殖細胞に特異的に発現している遺伝子です。そのような遺伝子24個を、マウスの皮膚組織にある線維芽細胞に導入したところ、ES細胞と同レベルまで初期化され、分化能を持つ細胞の樹立に成功しました。この細胞がiPS細胞です。
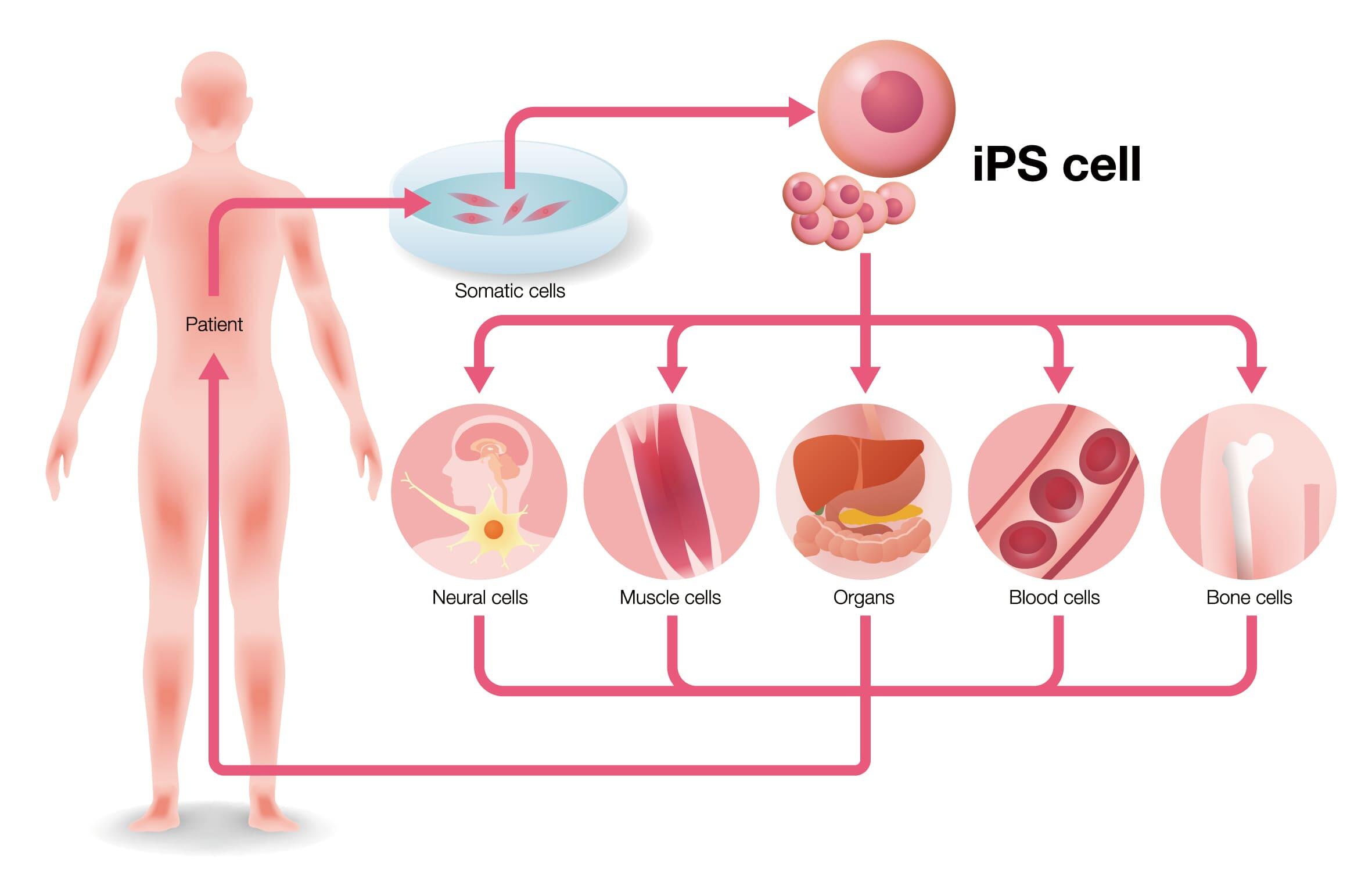
その後の研究で、細胞の初期化に必要な遺伝子は24個から4個までに絞り込まれます。(山中因子と呼ばれています)。そして、2007年ついにヒトiPS細胞の樹立に成功しました。iPS細胞もあらゆる細胞へ分化する機能を持ち、胚を破壊して作成するES細胞よりは倫理的問題は軽減されます。また、患者の体細胞からiPS細胞を作り出すこともでき、この方法を使った場合、拒絶反応の心配がないと考えられています。
※PSCには、上記のほかに、体細胞由来ES細胞(ntES細胞:nuclear transfer Embryonic Stem Cell)があります。皮膚などの体細胞の核を、核を取り除いた受精前の卵子に移植し、そこから胚を作り出すことで得られます。患者自身の体細胞の核を使えば拒絶反応が起きないと考えられていますが、卵子を必要とするため、ES細胞と同様、使用には慎重さが求められます。
幹細胞の医療応用
以上、幹細胞の特性と種類を見てきました。ここからは医療への応用例と現在行われている主な研究について紹介します。
先に見てきたように、幹細胞には、自己複製能と分化能があることが特徴でした。
このふたつの特徴により、幹細胞を目的の細胞に分化させ、培養して任意の組織を作製することができます。それらを損傷した部位に移植すると、体内で有効に働き、機能を取り戻すことができると言われています。こうした治療法が再生・細胞医療です。脳や中枢神経、軟骨、心筋など、一度損傷すると根治治療が難しいと言われている部位にも適用できるとされており、実用化に向けて安全性と有効性を確かめる臨床試験が多数実施されています。
以下、まず体内に元から存在する体性幹細胞の臨床応用研究を示します。
造血幹細胞:
骨髄の中で血球をつくりだすもとになっている細胞です。もともと幹細胞を用いた治療は、1950年代に血液の疾患に対して、造血幹細胞を移植したのが始まりです。移植医療としての骨髄移植(造血幹細胞移植)は現在でも活発に実施されていますが、再生医療等製品(細胞医薬品ともいう。細胞に何らかの加工を施して作製した医薬品)という意味では、2021年時点ではまだ認可された製品はありません。血液がんや血液系の難病を対象にした臨床試験が進められています。
間葉系幹細胞:
間葉系幹細胞(MSC:mesenchymal stem cell)は中胚葉系の骨芽細胞、脂肪細胞、筋細胞、軟骨細胞などだけではなく、内胚葉系の内臓組織や外胚葉系の神経などの細胞にも分化する能力を持つため、生活習慣病をはじめ、難病・希少疾患など、様々な疾患の治療に役立てることができます。成人の骨髄、脂肪組織や歯髄などからも比較的容易に得ることができるため臨床応用がしやすく、すでに発売されている製品が複数あります。免疫抑制作用を持つことや腫瘍に集積する性質があることも報告されており、移植後の拒絶防止や、がんの遺伝子治療薬の運び屋として利用する研究も行われています。
<製品例>
販売名【ステミラック注】:患者の間葉系幹細胞を抽出して培養することで何倍にも増加させ、患者の体に注入することで損傷した脊髄を再生させる治療薬。
組織幹細胞:
組織や臓器で失われた細胞の代わりを作る細胞です。組織・臓器の幹細胞は、循環器などに発生する生活習慣病を中心に臨床試験が進められています。すでに複数の細胞医薬品が日本でも販売されています。
<製品例>
販売名【ジェイス】:ヒト(自己)表皮由来細胞シート。やけどの治療に用いる。患者自身の表皮細胞をシート状に培養し適用すると、2~5年以内に正常皮膚の形態に似た複雑な表皮突起が構築される。
販売名【ハートシート】:患者の太ももの筋肉から採取した細胞(骨格筋芽細胞シート)から作った心筋細胞をシート状に培養して移植。心筋を再生させ、心不全を改善する。
ヒト多能性幹細胞(iPS細胞とヒトES細胞)が注目されている理由
再生医療等製品として認可されたものはまだない(2023年時点)
体性幹細胞がすでに実用化された製品があるのに対し、人工多能性幹細胞にはまだ実用化された製品はありません。しかし、再生医療の切り札として期待されているのには理由があります。
それは、体性幹細胞から作れる組織が限定的であるのに対し、多能性幹細胞はその名の通り、さまざまな組織・臓器に分化が可能で、さらに増殖力が強い(無限に増殖する)という点です。
現時点では安全性・技術面での課題(※)や倫理的な課題が残されており、その課題を克服しつつ、メリットを最大限生かすことのできる治療法の確立が急がれています。
※人工多能性幹細胞は、がん化のリスクが高く、更なるメカニズム解明と評価方法の確立が必要とされています。また、取り扱い(作製や目的の細胞への分化誘導、培養)には特別な技術が必要です。そのため、再現性が高く安全な培養方法の確立のための研究が盛んに行われています。公益財団法人京都大学iPS細胞研究財団(iPS財団)では、医療用グレードのiPS細胞「再生医療用iPS細胞ストック」を製造して、広く研究者に提供しています。自分自身の細胞は拒絶反応がありませんが、現状では培養にかかる時間や費用の面から、ストックされている細胞を使用する方が効率が良い場合が多いです。加齢性黄斑変性症 や網膜色素変性、心不全などの疾患に適用するための臨床試験が実施されています。
<ES細胞の臨床研究例>
日本では長年禁止されていたES細胞を使った研究ですが、2023年、国立成育医療研究センターが、重い肝臓病の赤ちゃんにES細胞から作り出した肝臓の細胞を移植する治験で、効果と安全性が確認できたと報告しています。
基礎研究・創薬研究での活用
ヒト多能性幹細胞は、基礎研究および創薬研究で積極的に利用が進んでいます。
ヒト多能性幹細胞が樹立される以前から、多能性幹細胞は、実験用細胞や実験用マウスの作製に用いられてきました。しかし、種の異なる動物での実験結果をヒトにそのまま当てはめることはできません。そのため、ヒトES細胞やヒトiPS細胞が樹立されたことの医学や創薬研究へのインパクトは計り知れないものがありました。立体的なミニ臓器(オルガノイド)を作製し、より実態に近いモデルで大量に実験することが可能となりつつあるのも、ヒト多能性幹細胞が人工的に作れるようになったからこそです。
特にiPS細胞は患者の細胞から作製することから、患者本人に合った薬を探すことに活用することができます。
<iPS創薬>
iPS細胞を創薬研究に生かす取り組みとして、理化学研究所バイオリソースセンター(理研BRC)を紹介します。患者の体細胞からつくったiPS細胞(疾患特異的iPS細胞)を集中的に保管管理しており、疾患種は231種類に及びます。この数は世界的に見ても最も充実したラインナップと言われており、いつでも必要な研究者が使用できるようになっています。この疾患特異的iPS細胞を使って見つけた新薬候補の臨床試験がすでに進行中です。動物実験の結果に問題がなくても、臨床試験でヒトに投与して初めて安全性や有効性の懸念が判明し実用化に至らない例は数多く存在します。iPS細胞で作製したモデルを使用することで事前検証の精度が高まり、臨床試験の成功確率が飛躍的に高まると期待されています。
まとめ
私たちの体は、たった1つの受精卵が増殖と分化を繰り返して作り上げられています。その大仕事を実現しているのが幹細胞です。成長したあとも、私たちの体がきちんと機能している裏には、常に分裂を繰り返し、失われた細胞を補ってくれる幹細胞の働きがあります。
生物がもともと持っていたこれらの幹細胞の機能を医療に応用することで、これまで治療が難しかった病気に対して、新たな方法を見つけることができるかもしれません。大きな可能性を秘めている幹細胞の研究に目が離せません。
記事執筆:吉田拓実(東京大学大学院 農学生命科学研究科 博士課程修了 博士(農学)/ 再考編集室 編集記者 / さいこうファーム 農場長)
(2024-2-13)